题目内容
【题目】物质检验、分离、提纯和制备是化学实验中的常见操作。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是______(用离子方程式表示)。
(2)检验食盐中所含阳离子的实验操作名称是_________。
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是_________。
(4)实验室制备氯气的化学反应方程式为_______,请在方程式中标出电子转移的方向和数目。
【答案】2Fe2++Cl2 = 2Fe3++2Cl-或2Fe2++H2O2+2H+ = 2Fe3++2H2O 焰色实验(或焰色反应) 酸性高锰酸钾溶液(或铁氰化钾溶液) 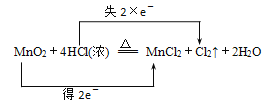
【解析】
(1)可以向混合液中通入氯气(或滴加双氧水)除去FeCl3溶液中混有的FeCl2,离子方程式:2Fe2++Cl2═2Fe3++2Cl﹣或2Fe2++H2O2+2H+═2Fe3++2H2O;
(2)检验食盐中所含阳离子的实验操作名称是焰色实验(或焰色反应),;
(3)亚铁离子具有还原性(或遇到铁氰化钾溶液产生蓝色沉淀),因此检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是酸性高锰酸钾溶液(或铁氰化钾溶液);
(4)浓盐酸与二氧化锰加热可制备氯气,Mn元素的化合价降低、Cl元素的化合价升高,则反应及转移电子方向和数目为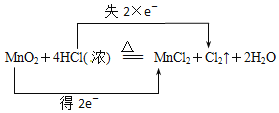 。
。

【题目】下列实验所得结论正确的是
① | ② | ③ | ④ |
|
|
|
|
充分振荡试管,下层溶液红色褪去 | 溶液变红 | 溶液变红 | 充分振荡右侧小试管, 下层溶液红色褪去 |
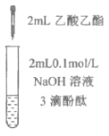
A.①中溶液红色褪去的原因是:CH3COOC2H5+NaOH![]() CH3COONa+C2H5OH
CH3COONa+C2H5OH
B.②中溶液变红的原因是:CH3COO-+H2O![]() CH3COOH+H+
CH3COOH+H+
C.由实验①、②、③推测,①中红色褪去的原因是乙酸乙酯萃取了酚酞
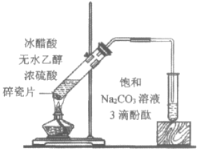
D.④中红色褪去证明右侧小试管中收集到的乙酸乙酯中混有乙酸
【题目】中国传统文化中包括许多科技知识。下列古语中不涉及化学变化的是
千淘万漉虽辛苦,吹尽狂沙始到金 |
熬胆矾(CuSO4·5H2O) 铁釜,久之亦化为铜 |
凡石灰(CaCO3), 经火焚炼为用 |
丹砂(HgS)烧之成水银,积变又成丹砂 |
A | B | C | D |
A. A B. B C. C D. D
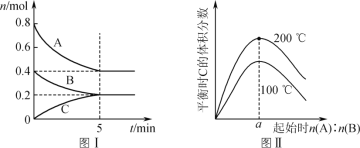
【题目】将一定量纯净的氨基甲酸胺(H2NCOONH4)固体,置于特制密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应: H2NCOONH4(s)![]() 2NH3(g)+CO2(g)达到分解平衡,实验测得不同温度及反应时间(t1<t2<t3)的有关表格:
2NH3(g)+CO2(g)达到分解平衡,实验测得不同温度及反应时间(t1<t2<t3)的有关表格:
氨基甲酸铵分解时温度、气体总浓度及反应时间的关系。
温度/℃ 气体总浓度(mol/L) 时间/min | 15 | 25 | 35 |
0 | 0 | 0 | 0 |
t1 | 0.9×10-3 | 2.7×10-3 | 8.1×10-3 |
t2 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
t3 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
(1)在25℃,0-t1时间内产生氨气的平均速率为___。
(2)根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)![]() H2NCOONH4(s)平衡常数K约为___。
H2NCOONH4(s)平衡常数K约为___。
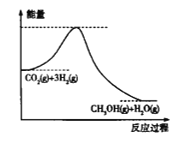
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:CO2(g)+3H2(g)![]() CH3OH(g)+H2(g) ΔH<0在恒温恒容的密闭容器中,加入1molCO2和3molH2,充分反应达平衡时放出热量akJ,若在原容器中加入2molCO2和6molH2,在相同温度下反应达平衡时放热bkJ,则a和b满足的关系___。
CH3OH(g)+H2(g) ΔH<0在恒温恒容的密闭容器中,加入1molCO2和3molH2,充分反应达平衡时放出热量akJ,若在原容器中加入2molCO2和6molH2,在相同温度下反应达平衡时放热bkJ,则a和b满足的关系___。