��Ŀ����
����Ŀ��ij��ɫ�����ĩ��Ʒ���ܺ���Fe2O3��Cu2O�е�һ�ֻ����֣�ijУ��ѧ����̽��ʵ��С���������ɽ���̽����
�������ϣ�Cu2O��������Һ�лᷢ����Ӧ��Cu2O+2H+=Cu+Cu2++H2O
̽��һ������ͼ��ʾװ�ý���ʵ�飬�ش��������⣺
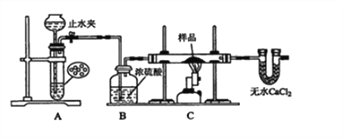
��1��������װ��ɺк�ֹˮ�У�______________________ ����˵��װ��A��������������
��2��װ��A�������ķ���װ�ã�����ѡ�õ�ҩƷ��______����ѡ�
A��ϡ�����пƬ B��ϡ�������Ƭ
C������������Һ����Ƭ D��Ũ�����þƬ
��3��������ʵ�鲽���У�ѡ����ȷ�IJ���˳����____________��������ţ���
����ֹˮ��
��Ϩ��C���ľƾ����
��C����ȴ�����ºر�ֹˮ��
����ȼC���ľƾ����
���ռ��������鴿
��ͨ������һ��ʱ�䣬�ž�װ���ڵĿ���
̽������
��4����ͬѧȡ������Ʒ���Թ��У�����������ϡ���ᣬ����ɫ�������ɣ���˵����Ʒ�в���Cu2O����ͬѧ��Ϊ�۵㲻��ȷ����ԭ����_____________(�����ӷ���ʽ��ʾ)����ͬѧ��ȡ������Ʒ���Թ��У�����������Ũ���ᣬ��������ɫ�����壮֤����Ʒ��һ������________���䷴Ӧ�����ӷ���ʽΪ_____����ͬѧ���ʵ��֤����һ�������Ƿ���ڣ�������Ʒ����м�����һ�����������Լ�����Ϊ______________��
��5��ȡһ������Ʒ���ձ��У�����������ϡ���ᣬ����Ӧ���˵õ�����3.2g����Һ��Fe2+��1.0mol������Ʒ��n��Cu2O��=_________mol��
���𰸡� ��װ��A�еij���©����ע��Һ�����γ�һ��Һ������Һ���߶ȱ��ֲ��� AC �ޢݢܢ� 2Fe3++Cu =2 Fe2++Cu2+ Cu2O Cu2O+6H++2NO3-=2Cu2++2NO2+3H2O ���� ���軯�� 0.55
��������(1)������װ��ɺк�ֹˮ�У��ڳ���©���м�ˮ�γ�һ��ˮ�����Ҳ������仯֤����������ã���װ��A�еij���©����ע��Һ�����γ�һ��Һע����Һ���߶ȱ��ֲ��䣬�ʴ�Ϊ����װ��A�еij���©����ע��Һ�����γ�һ��Һע����Һ���߶ȱ��ֲ��䣻
(2)�ɷ�Ӧԭ�����������ʿ�֪��ϡ���п��Ӧ������������������ǿ����Һ��Ӧ����������A��ϡ�����пƬ��Ӧ��������п����������A���ϣ�B��ϡ�������Ƭ��Ӧ������������һ��������ˮ������������������B�����ϣ�C������������Һ����Ƭ��Ӧ����ƫ�����ƺ���������C���ϣ�D��Ũ�����þƬ��Ӧ��������þ�����������ˮ����D�����ϣ��ʴ�Ϊ��AC��
(3)�������п������ȷ�����ը�����Կ�ʼ��ͨ��������ֹˮ������������ͨ������װ�ó���������Ŀ�����ų�װ���еĿ������������U�ܳ����������������ȣ����崿�����ٵ�ȼC���ľƾ���ƣ���Ӧ��ɺ��ȳ��ƾ��ƣ���������ȴ��ͣ����������λϨ��C���ľƾ���ƣ���C����ȴ�����ºر�ֹˮ�У���ֹ���ɵ�ͭ��������������������ȷ�Ĵ���˳��Ϊ���٢ޢݢܢڢۣ��ʴ�Ϊ���ޢݢܢ���
(4)ȡ������Ʒ���Թ��У�����������ϡ���ᣬ����ɫ�������ɣ��������������ܽ����ɵĺ�ɫͭ������֤����Ʒ�в���Cu2O����Ӧ�����ӷ���ʽΪ��2Fe3++Cu=2Fe2++Cu2+����ȡ������Ʒ���Թ��У�����������Ũ���ᣬ��������ɫ�����壬������ͭ�������Դ��������ӣ�֤����Ʒ��һ������Cu2O��������ͭ��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Cu2O+6HNO3(Ũ)=2Cu(NO3)2+2NO2��+3H2O�����ӷ���ʽΪCu2O+6H++2NO3-=2Cu2++2NO2+3H2O��Ҫ���ʵ��֤����һ�������������Ƿ���ڣ���Ҫ���������Ὣ�����ܽ⣬Ȼ�����������Ӻ����軯����Һ��Ӧ����Ѫ��ɫ��Һ��ƣ����������軯����Һ���ɫ��֤�����������ӣ������������ӣ��ʴ�Ϊ��2Fe3++Cu =2 Fe2++Cu2+��Cu2O��Cu2O+6H++2NO3-=2Cu2++2NO2+3H2O�����ᡢ���軯�أ�
(5)2Fe3++Cu=Cu2++2Fe2+��Cu2O+2H+�TCu+Cu2++H2O������Ϊͭ��������ȫ����Ӧ�����������ӣ�����1.0molFe2+������Cu0.5mol��ʣ��Cu���ʵ���=![]() =0.05mol��ԭ��Ʒ��Cu2O���ʵ���=0.05mol+0.5mol=0.55mol���ʴ�Ϊ��0.55��
=0.05mol��ԭ��Ʒ��Cu2O���ʵ���=0.05mol+0.5mol=0.55mol���ʴ�Ϊ��0.55��

 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�