题目内容
【题目】(1)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为______;若XY2为共价化合物时,其结构式为_____。
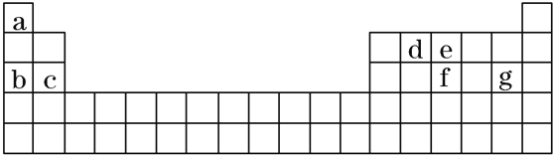
(2)现有a~g7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:
①元素的原子间反应最容易形成离子键的是_____(填序号,下同),容易形成共价键的是___。
A.c和f B.b和g C.d和g D.b和e
②写出a~g7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式___。
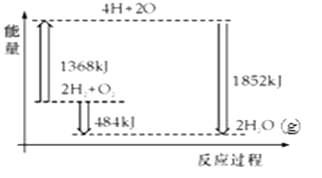
(3)将2moH2O和2molCO置于1L容器中,在一定条件下加热至高温,发生如下可逆反应:2H2O(g)![]() 2H2(g)+O2(g)、2CO(g)+O2(g)
2H2(g)+O2(g)、2CO(g)+O2(g)![]() 2CO2(g)。
2CO2(g)。
①当上述系统达到平衡时,欲求其混合气体的平衡组成。则至少还需婴知道两种气体的平衡浓度,但这两种气体不能同时是______或______。
②若平衡时O2和CO2的物质的量分别为n(O2)甲=amol,n(CO2)甲=bmol。试求n(H2O)甲=_____(用含a、b的代数式表示)。
【答案】 ![]() S=C=S B C CCl4(或PCl3) H2,H2O CO,CO2 (2-2a-b)mol
S=C=S B C CCl4(或PCl3) H2,H2O CO,CO2 (2-2a-b)mol
【解析】(1)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,为CaF2;若XY2为共价化合物时,为CS2;
(2)由元素的位置可知,a为H,b为Na,c为Mg,d为C,e为N,f为P,g为Cl,结合元素周期律和有关物质的结构与性质解答;
(3)①两个反应通过O2联系起来,只要知道O2和另外任意一种气体的平衡浓度,均可求出混合气体的平衡组成;
②根据方程式结合质量守恒计算。
(1)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,则为CaF2,其电子式为![]() ;若XY2为共价化合物时,则为CS2,其结构式为S=C=S;
;若XY2为共价化合物时,则为CS2,其结构式为S=C=S;
(2)由元素的位置可知,a为H,b为Na,c为Mg,d为C,e为N,f为P,g为Cl,则
①活泼的金属与活泼的非金属之间容易形成离子键,则元素的原子间反应最容易形成离子键的是b和g(NaCl),容易形成共价键的是d和g(CCl4),答案为:B;C;
②所有原子都满足最外层为8电子结构,不含H,化合物中中心元素的族序数+成键数=8可满足题意,则所有原子都满足最外层为8电子结构的任意一种分子的分子式为CCl4(或PCl3)。
(3)①由两个方程式可知,两个反应通过O2联系起来,只要知道O2和另外任意一种气体的平衡浓度,均可求出混合气体的平衡组成,当知道H2O和H2或CO和CO2的平衡浓度时,由于两个方程式无法通过O2建立反应量的关系,所以无法求其混合气体的平衡组成,因而不能是这两组,即答案为H2O、H2;CO、CO2;
②因n(CO2)甲=bmol,由方程式2CO(g)+O2(g)![]() 2CO2(g)可知平衡时反应的O2为b/2mol,则反应2H2O(g)
2CO2(g)可知平衡时反应的O2为b/2mol,则反应2H2O(g)![]() 2H2(g)+O2(g)中生成O2的物质的量为(a+b/2)mol,消耗的水为2×(a+b/2)mol=(2a+b)mol,所以n(H2O)甲=2mol-(2a+b)mol=(2-2a-b)mol。
2H2(g)+O2(g)中生成O2的物质的量为(a+b/2)mol,消耗的水为2×(a+b/2)mol=(2a+b)mol,所以n(H2O)甲=2mol-(2a+b)mol=(2-2a-b)mol。

【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点231.9C)与Cl2 反应制备SnCl4装置如下图所示。
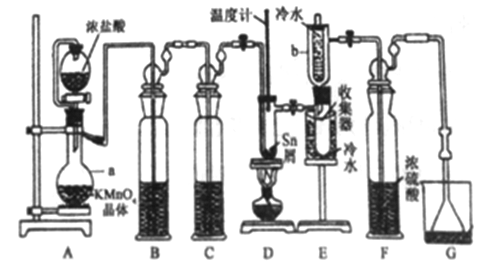
已知,① SnCl4在空气中极易水解生成SnO2xH2O;②SnCl2、SnCl4有关物理性质如下表。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
回答下列问题:
(1)仪器a的名称是__________,其中发生反应的离子方程式为________。
(2)装置B、C 中盛装的试剂分别是_______、__________。
(3)当观察到装置F液面上方出现_____现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的有:①加快氯气与锡反应,②__________。
(4)E装置中b的作用是___________。
(5)若制得产品中含有少量Cl2,则可采用下列_____(填字母)措施加以除去。
A.加入NaOH 萃取分液 B.加入足量锡再加热蒸馏
C.加入碘化钾冷凝过滤 D.加入饱和食盐水萃取
(6)可用滴定法测定最后产品的纯度。准确称取该样品mg加入到适量浓盐酸溶解,然后再加水稀释至250 mL,用移液管移取25.00 ml,稀释后的溶液于锥形瓶中,加入两滴淀粉溶液作指示制,用cmol/L 的KIO3 标准溶液进行滴定,平行滴定3 次,平均消耗V mL的标准溶液。已知滴定时发生的反应为:Sn2++IO3-+H+→Sn4++I2+H2O(未配平)。回答下列问题:
①判断达到滴定终点的现象为____________。
②产品中SnCl2(摩尔质量为M g/mol )的含量为____%(用含m、c、V、M 的代数式表示)。