题目内容
9.下列反应的离子方程式书写正确的是( )| A. | 过量铁加入到稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO2↑+4H2O | |
| B. | 向AgCl悬浊液中滴加饱和KI溶液 AgCl+I-═AgI+Cl- | |
| C. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+H2O═2Al(OH)3↓+HCO3- | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
分析 A.铁与稀硝酸反应生成硝酸亚铁和NO气体;
B.碘化银的溶解度小于氯化银,实现了沉淀的转化;
C.离子方程式两边负电荷不相等,违反了电荷守恒;
D.澄清石灰水过量,反应后不会剩余碳酸根离子.
解答 解:A.过量铁加入到稀硝酸中,反应生成硝酸亚铁和NO,正确的离子方程式为:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,故A错误;
B.向AgCl悬浊液中滴加饱和KI溶液,氯化银沉淀转化成碘化银,反应的离子方程式为:AgCl+I-═AgI+Cl-,故B正确;
C.向NaAlO2溶液中通入过量CO2,反应生成氢氧化铝沉淀和碳酸氢钠,正确的离子方程式为:2AlO2-+2CO2+4H2O═2Al(OH)3↓+2HCO3-,故C错误;
D.NaHCO3溶液中加入过量的澄清石灰水,反应生成碳酸钙沉淀、水和氢氧化钠,反应的离子方程式为:2HCO3-+2Ca2++2OH-═2CaCO3↓+2H2O,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
相关题目
7.一定条件下,对于含有一定数目分子的气体,决定其体积的主要因素是( )
| A. | 气体分子间的平均距离 | B. | 气体的分子的形状 | ||
| C. | 气体分子本身的大小 | D. | 气体分子的种类 |
17.物质的量浓度相同的下列溶液中,含粒子种类最多的是( )
| A. | K2CO3 | B. | CH3COONa | C. | NH4Cl | D. | CaCl2 |
4.下列有关金属的腐蚀的说法中,不正确的是( )
| A. | 纯银饰品久置表面变暗属于化学腐蚀 | |
| B. | 温度越高,金属发生化学腐蚀的速率越快 | |
| C. | 金属腐蚀就是金属失去电子被氧化的过程 | |
| D. | 铁门上的铜铆钉处在潮湿的空气中直接发生反应:Fe-3e-═Fe3+ |
1.现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)某同学根据上述信息,所画的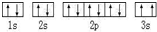 B电子排布图如图,违背了泡利原理.
B电子排布图如图,违背了泡利原理.
(3)CD3中心原子的杂化方式为sp3,分子立体构型三角锥形形.
(4)E元素基态原子的电子占用15个原子轨道,有26种不同运动状态.
(5)F元素的元素符号为As,其基态原子的核外电子排布式1s22s22p63s23p63d104s24p3.
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E元素的+3价离子有5个未成对电子 |
| F在周期表的第15列 |
(2)某同学根据上述信息,所画的
 B电子排布图如图,违背了泡利原理.
B电子排布图如图,违背了泡利原理.(3)CD3中心原子的杂化方式为sp3,分子立体构型三角锥形形.
(4)E元素基态原子的电子占用15个原子轨道,有26种不同运动状态.
(5)F元素的元素符号为As,其基态原子的核外电子排布式1s22s22p63s23p63d104s24p3.
18.在氨水中存在电离平衡:NH3•H20?NH4++OH-,下列说法错误的是( )
| A. | 向氨水中通入HCl气体,溶液导电性增强 | |
| B. | 向氨水中加入水,$\frac{{C}_{(O{H}^{-})}}{N{H}_{3}•{H}_{2}O}$值增大 | |
| C. | 向氨水中通入NH3,电离度增大 | |
| D. | 向氨水中加入水,Kb不变 |
19.0.5mol K2SO4中所含的K+离子数为( )
| A. | 3.01×1023 | B. | 6.02×1023 | C. | 0.5 | D. | 1 |
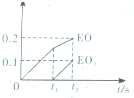 将E单质缓慢通入石灰水中,若生成物中有三种含E元素的离子,其中两种离子的物质的量与反应时间的曲线如图所示,则t1时刻[n(EO-)=0.15mol]消耗氢氧化钙的物质的量为0.15mol,t2时总反应的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.
将E单质缓慢通入石灰水中,若生成物中有三种含E元素的离子,其中两种离子的物质的量与反应时间的曲线如图所示,则t1时刻[n(EO-)=0.15mol]消耗氢氧化钙的物质的量为0.15mol,t2时总反应的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.