题目内容
17.物质的量浓度相同的下列溶液中,含粒子种类最多的是( )| A. | K2CO3 | B. | CH3COONa | C. | NH4Cl | D. | CaCl2 |
分析 根据物质在水溶液中电离程度和水解确定溶液中存在的微粒,根据微粒种类多少判断即可.
解答 解:A.碳酸钾溶液中碳酸根离子分步水解,所含粒子为K+、CO32-、HCO3-、H2CO3、H2O、H+、OH-,共7种粒子;
B.CH3COONa溶液中,CH3COO-水解,所含粒子为CH3COO-、Na+、H2O、H+、OH-、CH3COOH,共6种粒子;
C.NH4Cl水溶液中含有H+、OH-、NH3•H2O、NH4+、H2O、Cl-故6种粒子;
D.CaCl2溶液中所含粒子为Ca2+、Cl-、H2O、H+、OH-,共5种粒子;
上述溶液中K2CO3溶液中含有粒子数最多;
故选A.
点评 本题考查了盐类水解,根据盐类水解特点结合溶液中存在的微粒种类分析解答,知道多元弱酸根离子要分步水解,知道多元弱酸和多元弱碱水解的区别,题目难度不大.

练习册系列答案
相关题目
15.下列物质属于弱电解质的是( )
| A. | NaCl | B. | NaOH | C. | CH3COOH | D. | CO2 |
5.下列对于“摩尔”的理解正确的是( )
| A. | 摩尔是国际单位制的一个基本物理量 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 | |
| D. | 表示6.02×1023个粒子的集合体 |
12.下列说法正确的是( )
| A. | 1mol Cl2与足量Fe反应,转移电子的物质的量为3mol | |
| B. | 工业可采用火法炼铜:Cu2S+O2═2Cu+SO2,每生成2mol铜,反应共转移6mol电子 | |
| C. | 称取25g CuSO4•5H2O固体溶于75g水中,所得溶液中溶质的质量分数为25% | |
| D. | NO和NO2的混合气体共1mol,其中氮原子数为2mol |
2.下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①氨基酸 ②蛋白质 ③Al(OH)3 ④Al2O3 ⑤AlCl3 ⑥Al.
①氨基酸 ②蛋白质 ③Al(OH)3 ④Al2O3 ⑤AlCl3 ⑥Al.
| A. | 除②以外 | B. | 除⑤以外 | C. | 除⑥以外 | D. | 全部 |
9.下列反应的离子方程式书写正确的是( )
| A. | 过量铁加入到稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO2↑+4H2O | |
| B. | 向AgCl悬浊液中滴加饱和KI溶液 AgCl+I-═AgI+Cl- | |
| C. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+H2O═2Al(OH)3↓+HCO3- | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |

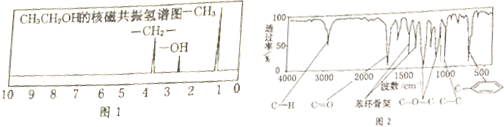
 或
或 .
. .
.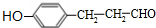 等.
等.