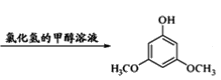
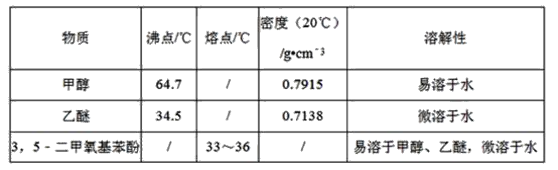
��Ŀ����
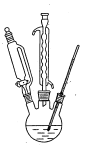
����Ŀ���⻯��(CaH2)������һ�ִ�����ϣ���ˮ��Ӧ�����������ƺ��������ǵ�ɽ�˶�Ա���õ���Դ�ṩ����ij��ѧ��ȤС�������ȡ�⻯�Ƶ�װ������(�̶�װ������ȥ)������˵������ȷ����
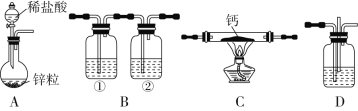
A.װ��A����ȡH2�����ӷ���ʽΪZn��2H����Zn2����H2��
B.װ��B�����ڳ�ȥH2�����ʣ�����ʢ��NaOH��Һ������ʢ��Ũ����
C.װ��C����ȡCaH2���ȵ�ȼC���ƾ��ƣ����A�з�Һ©���Ļ���
D.װ��D����ֱ���ܵ�������ƽ��ѹǿ���۲�H2�����Ե��ڷ�Ӧ�Ľ���
���𰸡�C
��������
װ��Aϡ�����п��Ӧ��ȡ������Bװ�ó�ȥ�����е�HCl�����ˮ������װ��CΪ��Ӧ����װ�ã���ȡ�⻯�ƣ�װ��D���ڹ۲�H2�����Ե��ڷ�Ӧ�Ľ��С�
A. װ��A��ϡ�����п��Ӧ��ȡ���������ӷ���ʽΪZn��2H����Zn2����H2������A��ȷ��
B. װ��B�����ڳ�ȥH2�����ʣ����ȳ�HCl�����ٳ�ˮ�����ʢ���ʢ��NaOH��Һ������ʢ��Ũ���ᣬ��B��ȷ��
C. װ��C����ȡCaH2�����ȴ�A�з�Һ©���Ļ���һ��ʱ����ȼC���ƾ��ƣ���ֹ����������Ӧ����������������ը����C����
װ��D����ֱ���ܵ�������ƽ��ѹǿ���۲�H2�����Ե��ڷ�Ӧ�Ľ��У���D��ȷ��
�ʴ�ѡ��C��

����Ŀ����ҵ�ϳ�������ʯ����Ҫ�ɷ�3BeOAl2O36SiO2����������Ԫ�أ�ұ���룬��Ĺ���������ͼ��ʾ��
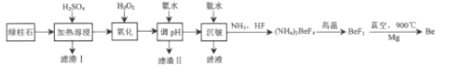
��֪��Be��Al�������ƣ����ֽ��������ӵ������������ʱ��pH�����
Be2+ | Al3+ | Fe3+ | Fe2+ | |
��ʼ����ʱ | 5.2 | 3.3 | 1.5 | 6.5 |
������ȫʱ | 8.8 | 5.0 | 3.7 | 9.7 |
�ش��������⣺
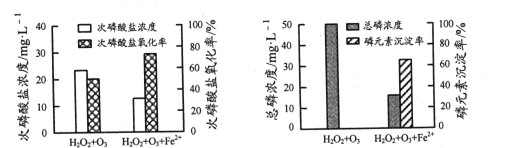
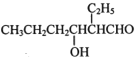
��1�����������Ҫ�ɷ���______������H2O2��������______��
��2���õ�������ĺ���pH��Χ��______��
��3���û�ѧ����ʽ���Ͳ���ʹ��NaOH��Һ�������ԭ����______��
��4���õ���NH4��2BeF4�Ļ�ѧ����ʽΪ______��
��5����Mg��ԭBeF2�õ�Be��Ҫ��յĻ�������ԭ����______��
��6��������ʯ��BeO�ĺ���Ϊa%��1������ʯ����������2%�ĺϽ�b�֣���Be��������Ϊ______�����ú�a��b�ı���ʽ��ʾ��