题目内容
15.下列变化中属于原电池反应的是( )| A. | 铁锈可用稀盐酸洗去 | |
| B. | 在空气中金属铝表面迅速被氧化形成保护膜 | |
| C. | 在Fe与稀H2SO4反应时,加几滴CuSO4溶液,可加快反应速率 | |
| D. | 红热的铁丝与水接触表面形成蓝黑色保护层 |
分析 属于原电池反应,说明符合原电池的构成条件,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,以此解答.
解答 解:A、铁锈可用稀盐酸洗去是因为铁锈Fe2O3是碱性氧化物,与HCl反应生成FeCl3和水,没有形成原电池,故A错误;
B、金属铝是比较活泼的金属,在空气中放置的时候能与氧气反应,表面迅速被氧化形成致密的保护膜,与原电池无关,故B错误;
C、加几滴CuSO4溶液后,铁与CuSO4反应生成单质Cu,然后铁和铜在稀H2SO4溶液中形成原电池,加快了铁与稀H2SO4的反应速率,故C正确;
D、红热的铁丝和水直接反应生成黑色的四氧化三铁和氢气,不符合原电池构成条件,属于化学腐蚀,故D错误;
故选C.
点评 本题考查了电化学腐蚀的判断,为高频考点,侧重于学生的分析能力的考查,根据原电池构成条件来分析解答即可,难度不大.

练习册系列答案
相关题目
1.如图是某有机物核磁共振氢谱图,但该物质可能是( )
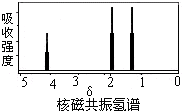

| A. | CH3COOCH2CH3 | B. | CH3CH=CHCH3 | C. | CH3CH2CH3 | D. | CH3CHOHCH3 |
6.五氧化二钒广泛用于冶金、化工等行业,主要用于冶炼钒铁.用作合金添加剂,占五氧化二钒总消耗量的80%以上,其次是用作有机化工的催化剂.为了增加V2O5的利用率,我们从废钒催化剂(主要成分V2O5,VOSO4,K2SO4,SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:
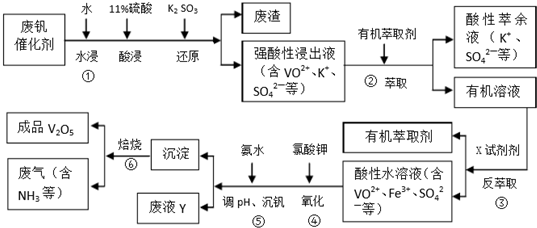
回答下列问题:
(1)①中废渣的主要成分是SiO2.
(2)②,③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):R2(SO4)n(水层)+2nHA(有基层)?2RA(有基层)+nH2SO4(水层).②中萃取时必须加入适量碱,其原因是加入碱中和硫酸使平衡正移、多次连续萃取,提高钒的萃取率;实验室进行萃取操作主要使用的玻璃仪器为分液漏斗和烧杯.
(3)完成④中反应的例子方程式:1ClO3-6VO2++6H+=6VO3+1Cl-+3H2O
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间的关系如下表:
试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为1.7;若钒沉淀率为93.1%时不产生Fe(OH)3,沉淀,则此时溶液中c(Fe3+)=2.6×10-3mol/L.(已知:25℃时k[Fe(OH)3]=2.6×10-39.)

回答下列问题:
(1)①中废渣的主要成分是SiO2.
(2)②,③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):R2(SO4)n(水层)+2nHA(有基层)?2RA(有基层)+nH2SO4(水层).②中萃取时必须加入适量碱,其原因是加入碱中和硫酸使平衡正移、多次连续萃取,提高钒的萃取率;实验室进行萃取操作主要使用的玻璃仪器为分液漏斗和烧杯.
(3)完成④中反应的例子方程式:1ClO3-6VO2++6H+=6VO3+1Cl-+3H2O
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间的关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 | 89.3 |
10.已知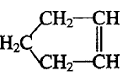 可简写为
可简写为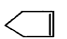 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: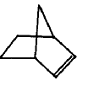
则降冰片烯不具有的性质( )
 可简写为
可简写为 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为:
则降冰片烯不具有的性质( )
| A. | 易溶于水 | B. | 能发生氧化反应 | C. | 能发生加成反应 | D. | 能发生取代反应 |
20.下列叙述中正确的是( )
| A. | 化学反应中物质变化的实质是旧化学键的断裂和新化学键的形成 | |
| B. | 离子化合物中一定有金属元素和非金属元素 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 共价化合物中各原子都一定满足最外层8电子稳定结构 |
7.下列过程吸收能量的是( )
| A. | 钠与水反应 | B. | H+H→H2 | C. | 石灰石分解 | D. | 酸碱中和 |
5.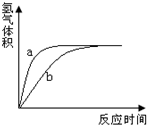 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )| A. | a表示水,b表示无水乙醇 | B. | a表示无水乙醇,b表示水 | ||
| C. | 都可用a曲线表示 | D. | 都可用b曲线表示 |