题目内容
5.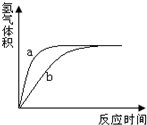 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )| A. | a表示水,b表示无水乙醇 | B. | a表示无水乙醇,b表示水 | ||
| C. | 都可用a曲线表示 | D. | 都可用b曲线表示 |
分析 质量和形状相同的两小块金属钠分别加入足量水和足量无水乙醇中,因水和无水乙醇足量,则生成的氢气相同,但乙醇和水的性质不同,乙醇中含有羟基,能与金属钠反应生成氢气,比在水中反应安静,并不剧烈,缓缓产生气泡,据此分析解答;
解答 解:由图象可知,横坐标为时间,纵坐标为生成氢气的体积,将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,排除了接触面积等影响反应速率的因素,2Na+2H2O=2NaOH+H2↑;2Na+2C2H5OH=2C2H5ONa+H2↑,根据方程可知同质量的钠分别与足量的水、乙醇最终两者产生的氢气一样多;乙醇为非电解质,水为弱电解质,H的活泼性顺序:水>乙醇,所以钠在水反应速率大于乙醇,所以a表示水,b表示无水乙醇,故A正确;
故选A.
点评 本题考查化学反应及图象,明确图象中氢气的体积及反应速率是解答的关键,注意乙醇中含有羟基,能与金属钠反应生成氢气,但乙醇中羟基的O-H键比水难以断裂,比在水中反应安静,题目难度不大.

练习册系列答案
相关题目
15.下列变化中属于原电池反应的是( )
| A. | 铁锈可用稀盐酸洗去 | |
| B. | 在空气中金属铝表面迅速被氧化形成保护膜 | |
| C. | 在Fe与稀H2SO4反应时,加几滴CuSO4溶液,可加快反应速率 | |
| D. | 红热的铁丝与水接触表面形成蓝黑色保护层 |
16.近20年来,同位素分析法在植物生理学、生态学和环境科学研究中获得广泛应用;如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境指示物.下列有关说正确的是( )
| A. | 34S原子核内中子数为16 | B. | 1H218O的摩尔质量为20g/mol | ||
| C. | 13C和15N原子核内的质子数相差2 | D. | 2H+的核外电子数为2 |
13.乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
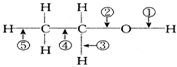

| A. | 和金属钠作用时,键①断裂 | |
| B. | 和浓H2SO4共热至170℃时,键②和⑤断裂 | |
| C. | 在Ag催化剂下和O2反应时,键①和③断裂 | |
| D. | 和CH2COOH共热时,键②断裂 |
20.下列烷烃化合物中,只有两种同分异构体的是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
17.用NA表示阿佛加德罗常数,下列说法中正确的是( )
| A. | 1摩铜作还原剂一定提供NA个电子 | |
| B. | 64克二氧化硫中含有NA个氧分子 | |
| C. | 标准状况下,22.4升氨气中含有3NA个氢原子 | |
| D. | 18克重水中含有10NA个电子 |
14.在一定温度下,某固定容积的密闭容器中发生如下反应2NO2?2NO+O2.此反应达到平衡状态的标志是( )
| A. | NO2、NO、O2的物质的量浓度之比为2:2:1 | |
| B. | 单位时间内生成n mol O2,同时消耗2n mol NO2 | |
| C. | 混合气体的平均摩尔质量不再改变 | |
| D. | 正反应和逆反应都已停止 |
15.如图示为一种天然产物,具有一定的除草功效.下列有关该化合物的说法错误的是( )
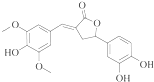

| A. | 分子中含有三种含氧官能团 | |
| B. | 1 mol该化合物最多能与6molNaOH反应 | |
| C. | 既可以发生取代反应,又能够发生加成反应 | |
| D. | 既能与FeC13发生显色反应,也能和Na2CO3反应 |