题目内容
10.已知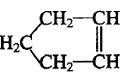 可简写为
可简写为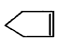 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: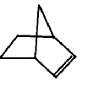
则降冰片烯不具有的性质( )
| A. | 易溶于水 | B. | 能发生氧化反应 | C. | 能发生加成反应 | D. | 能发生取代反应 |
分析 该分子中含有碳碳双键,具有烯烃的性质,能发生加成反应、加聚反应、氧化反应,含有亚甲基,能发生取代反应,据此分析解答.
解答 解:该分子中含有碳碳双键,具有烯烃的性质,能和溴及氢气等物质发生加成反应、能发生加聚反应生成高分子化合物、能被酸性高锰酸钾溶液等强氧化剂氧化,含有亚甲基,能发生取代反应,因为是有机物,所以不能溶解于水,故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系即可解答,侧重考查烯烃性质,以乙烯为里熟记烯烃性质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列关于元素周期表的说法正确的是( )
| A. | ⅠA族元素也称为碱金属元素 | |
| B. | 稀有气体元素原子的最外层电子数均为8 | |
| C. | 过渡元素全部是金属元素,因此它们又被称为过渡金属 | |
| D. | 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
1.某实验室小组偶然发现将镁条插入饱和NaHCO3溶液中,镁条表面出现大量气泡.为了探究产生此现象的原因,该小组设计实验探究如下:
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程在烧杯中加入足量的碳酸氢钠固体,加入适量蒸馏水,加热使之溶解,冷却后取上层清液即可.饱和NaHCO3溶液pH=8.4,用离子方程式表示HCO3-+H2O?H2CO3+OH-.
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同.表中不要留空格):
(3)对于反应中产生的气体(不考虑水蒸气),请你完成假设二和假设三:假设一:只有CO2;假设二:只有H2;假设三:H2和CO2;
请假设实验,用镁条和饱和NaHCO3溶液制取气体并检验其中是否含有CO2,写出实验步骤和结论.
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程在烧杯中加入足量的碳酸氢钠固体,加入适量蒸馏水,加热使之溶解,冷却后取上层清液即可.饱和NaHCO3溶液pH=8.4,用离子方程式表示HCO3-+H2O?H2CO3+OH-.
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同.表中不要留空格):
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将镁条投入5mL蒸馏水 | 微量气泡 | Mg与蒸馏水缓慢反应 |
| ② | 将镁条投入5mL饱和NaHCO3溶液中 | 镁表面出现大量气泡 | Mg与NaHCO3溶液剧烈反应 |
| ③ | 将镁条投入5mLNaOH溶液中 | 现象不明显 | Mg与NaOH溶液较难反应 |
请假设实验,用镁条和饱和NaHCO3溶液制取气体并检验其中是否含有CO2,写出实验步骤和结论.
| 实验步骤 | 想象和结论 |
| 大试管中加入擦去氧化膜的镁条 |
18.下列说法正确的是( )
①离子化合物一定含离子键,也可能含共价键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物.
①离子化合物一定含离子键,也可能含共价键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物.
| A. | ①③⑤ | B. | ②④⑥ | C. | ②③④ | D. | ①③⑥ |
15.下列变化中属于原电池反应的是( )
| A. | 铁锈可用稀盐酸洗去 | |
| B. | 在空气中金属铝表面迅速被氧化形成保护膜 | |
| C. | 在Fe与稀H2SO4反应时,加几滴CuSO4溶液,可加快反应速率 | |
| D. | 红热的铁丝与水接触表面形成蓝黑色保护层 |
19.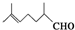 甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )
甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )
 甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )
甜瓜醛是调制西瓜、甜瓜、黄瓜、柠檬、苹果等味道的食用香精.其结构简式如图所示.下列有关甜瓜醛的叙述正确的是( )| A. | 该物质最多可与1 mol氢气发生加成反应 | |
| B. | 该物质的分子式为C9H14O | |
| C. | 加热条件下,该物质能与新制Cu(OH)2悬浊液反应 | |
| D. | 该物质为烯烃 |
20.下列烷烃化合物中,只有两种同分异构体的是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |