题目内容
在密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是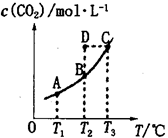
| A.平衡状态A与C相比,平衡状态A的c(CO)小 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
C.反应CO(g)+H2O(g) CO2(g)+H2(g)△H>0 CO2(g)+H2(g)△H>0 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
A
解析试题分析:A、平衡状态A与C相比,C点温度高,已知△H>0,升高温度平衡正移,CO浓度减小,所以A点CO浓度大,故A错误,B、T2时反应进行到状态D,c(CO)高于平衡浓度,故反应向逆反应进行,则一定有υ(正)<υ(逆),故B正确; C、由图可知,温度越高平衡时c(CO)越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应进行,故正反应是吸热反应,即△H>0,故C正确;D、该反应正反应是吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故K1<K2,故D正确;
考点:化学反应的平衡状态,平衡常数;

在容积不变的密闭容器中加入1 mol N2和3 mol H2发生反应,下列叙述正确的是
A.该反应的热化学方程式为:N2 + 3H2 2NH3ΔH =-92 kJ/mol 2NH3ΔH =-92 kJ/mol |
| B.达到平衡后向容器中通入1 mol氦气,平衡不移动 |
| C.曲线b表示可能使用了催化剂 |
| D.降低温度和缩小容器体积均可使该反应平衡常数增大 |
已知:CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH=-49.0 kJ?mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
CH3OH(g) + H2O(g) ΔH=-49.0 kJ?mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
A.10min后,升高温度能使 增大 增大 |
| B.反应达到平衡状态时,CO2的平衡转化率为75% |
| C.3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 |
| D.从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol·L-1?min-1 |
在某温度下,H2和I2各0.10mol的气态混合物充入10L的密闭容器中,发生反应:H2(g)+I2(g)  2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol?L-1,则该反应的平衡常数为( )
2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol?L-1,则该反应的平衡常数为( )
| A.40 | B.62.5 | C.0.25 | D.4 |
在一定温度下,将气体X和气体Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应X(g)+ Y(g)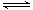 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表( )
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表( )
| t / min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10-5 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
已知2SO2 (g) + O2 (g)  2SO3 (g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3 (g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
| A.容器内压强P:P甲=P丙 > 2P乙 |
| B.SO3的质量m:m甲=m丙 > 2m乙 |
| C.c(SO2)与c(O2)之比k:k甲=k丙 > k乙 |
| D.反应放出或吸收热量的数值Q:Q甲=Q丙 > 2Q乙 |
氯气在298K、101kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。估算该反应的平衡常数( )
| A.5.4×10—5 | B.4.5×10—4 | C.0.015 | D.无法计算 |
对于可逆反应N2(g)+3H2(g)  2NH3(g) ΔH<0,下列研究目的和示意图相符的是
2NH3(g) ΔH<0,下列研究目的和示意图相符的是
| | A | B | C | D |
| 研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
| 示意图 |  | 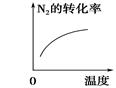 | 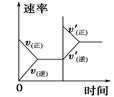 |  |
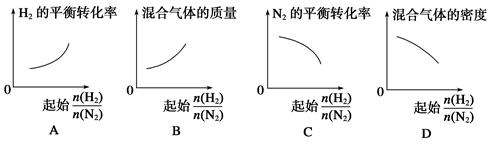
 2NH3。
2NH3。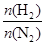 表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是( )
表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是( )