题目内容
对于可逆反应N2(g)+3H2(g) 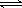 2NH3(g) ΔH<0,下列研究目的和示意图相符的是
2NH3(g) ΔH<0,下列研究目的和示意图相符的是
| | A | B | C | D |
| 研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
| 示意图 | 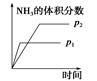 | 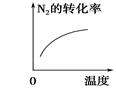 | 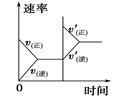 | 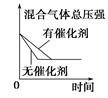 |
C
解析试题分析:A.增大压强,化学反应速率加快,达到平衡所需要的时间更少。P1>P2。错误。B.升高温度,化学平衡向吸热反应方向即向逆反应方向移动。N2的转化率降低。错误。C.平衡体系中增加N2的浓度。在这一瞬间,反应物的浓度突然增大,生成物的浓度不变,所以V(正)>V(逆).所以化学平衡向正反应方向移动,直至达到新的平衡。正确。D.加入催化剂,由于改变了反应途径,化学反应速率大大加快,缩短了达到平衡所需要的时间。错误。
考点:考查浓度、温度、压强、催化剂等外界条件对化学反应速率和化学平衡的影响的知识。

练习册系列答案
相关题目
判断一个化学反应的自发性常用焓判据和熵判据,则在下列情况下,可以判定反应一定自发进行的是
| A.ΔH>0,ΔS>0 | B.ΔH<0,ΔS>0 | C.ΔH>0,ΔS<0 | D.ΔH<0,ΔS<0 |
在密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是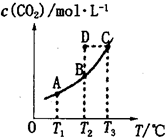
| A.平衡状态A与C相比,平衡状态A的c(CO)小 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
C.反应CO(g)+H2O(g) CO2(g)+H2(g)△H>0 CO2(g)+H2(g)△H>0 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
下列原理和定律中,可用于判断化学平衡移动方向的是
| A.盖斯定律 | B.阿伏加德罗定律 | C.勒夏特列原理 | D.质量守恒定律 |
一定温度下,向aL密闭容器中加入2mol NO2(g),发生如下反应:2NO2 2NO+O2,此反应达到平衡状态的标志是
| A.混合气体的密度不再变化 |
| B.混合气体的颜色变浅 |
| C.混合气体中NO2、NO、O2的物质的量之比为2:2:1 |
| D.单位时间内生成2n mol NO同时生成2n mol NO2 |
在一定温度下,向密闭容器中充入1.0molN2和3.0molH2,反应在一定压强下,达到平衡时测得NH3的物质的量为0.6mol。若在该容器中开始时充入2.0 molN2和6.0molH2,则平衡时NH3的物质的量为
| A.若为定容容器,n(NH3)=1.2mol | B.若为定压容器,n(NH3) >1.2mol |
| C.若为定容容器,n(NH3)>1.2mol | D.若为定压容器,n(NH3)<1.2mol |
 cC(g) ΔH ="Q" 在密闭容器中进行,在不同温度(T1 和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是
cC(g) ΔH ="Q" 在密闭容器中进行,在不同温度(T1 和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是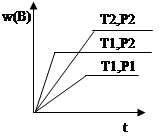
 4C(1)+2D( g)。平衡时测得n(C)="1.6mol" ,反应的化学平衡常数表达式为
4C(1)+2D( g)。平衡时测得n(C)="1.6mol" ,反应的化学平衡常数表达式为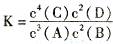
 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )