题目内容
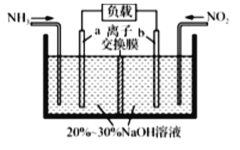
【题目】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(1)用双线桥表示出电子转移的方向和数目__,题干中反应改写成离子方程式是__。
(2)电解食盐水的过程中,被还原的元素是__,氧化产物是__。
【答案】 2Cl-+2H2O
2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑ 氢元素(或H) 氯气(或Cl2)
2OH-+Cl2↑+H2↑ 氢元素(或H) 氯气(或Cl2)
【解析】
(1)2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑反应中,氯元素化合价由-1升高为0,氢元素化合价由+1降低为0。元素化合价降低发生还原反应,元素化合价升高被氧化。
2NaOH+Cl2↑+H2↑反应中,氯元素化合价由-1升高为0,氢元素化合价由+1降低为0。元素化合价降低发生还原反应,元素化合价升高被氧化。
(1)2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑反应中,氯元素化合价由-1升高为0,氢元素化合价由+1降低为0,用双线桥表示出电子转移的方向和数目为
2NaOH+Cl2↑+H2↑反应中,氯元素化合价由-1升高为0,氢元素化合价由+1降低为0,用双线桥表示出电子转移的方向和数目为 ,2NaCl+2H2O
,2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑反应的离子方程式是2Cl-+2H2O
2NaOH+Cl2↑+H2↑反应的离子方程式是2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑;
2OH-+Cl2↑+H2↑;
(2)2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑反应,氢元素化合价由+1降低为0,所以被还原的元素是氢元素,氯元素化合价由-1升高为0,所以氧化产物是氯气。
2NaOH+Cl2↑+H2↑反应,氢元素化合价由+1降低为0,所以被还原的元素是氢元素,氯元素化合价由-1升高为0,所以氧化产物是氯气。

【题目】某温度下, 反应H2(g)+CO2(g)![]() H2O(g)+CO(g)的平衡常数
H2O(g)+CO(g)的平衡常数![]() 。该温度下在体积均为10 L的三个密闭容器中分别加入反应物,起始加入量如图所示:下列判断不正确的是
。该温度下在体积均为10 L的三个密闭容器中分别加入反应物,起始加入量如图所示:下列判断不正确的是
起始量 | 甲 | 乙 | 丙 |
H2 (mol) | 1 | 2 | 2 |
CO2(mol) | 1 | 1 | 2 |
A.反应开始时,甲中的反应速率最慢,丙中的反应速率最快
B.平衡时,甲和丙中CO2的转化率相等,均是60%
C.平衡时,乙中H2的转化率大于60%
D.平衡时,丙中c(H2 ) 是0. 08 mol·L-1
【题目】已知常温下浓度为0.lmol/L的下列溶液的pH如下表,下列有关说法正确的是( )
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序: H2CO3< HClO<HF
B.向上述NaC1O溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>(H+)>c(HClO) >c(OH-)
C.根据上表,水解方程式ClO-+H2O![]() HClO+OH-的水解常数K=10-7.6
HClO+OH-的水解常数K=10-7.6
D.若将CO2通入0.lmol/LNa2CO3溶液中至溶液中性,则溶液中2c(CO32-)+c(HCO3-)=0.1 mol/L