题目内容
5.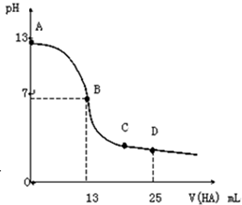 常温下,向25mL0.1mol•L-1MOH溶液中逐滴加入0.2mol•L-1HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
常温下,向25mL0.1mol•L-1MOH溶液中逐滴加入0.2mol•L-1HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:(1)写出MOH在水溶液中的电离方程式MOH═M++OH-.
(2)MOH与HA恰好完全反应时,溶液呈碱性(填“酸”、“碱”或“中”).用离子方程式表示其原因碱;A-+H2O?HA+OH-;此时,混合溶液中由水电离出的c(H+)>0.2mol•L-1HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(3)D点时,溶液中c(A-)+c(HA)=2c(M+)(填“>”“<”或“=”);若此时测得混合溶液的pH=3,则c(HA)+c(H+)=0.05+10-11 mol•L-1(数字表达式,不必具体算出结果).
(4)假设室温下,0.1mol•L-1HA在水中有0.1%发生电离,则该溶液的pH=4.
分析 (1)由图象可知0.1mol/L MOH溶液的pH=13,c(OH-)=0.1mol/L,说明为强碱,完全电离;
(2)由图象可知,当加入13mL 0.2mol/L HA溶液时,n(HA)=0.0026mol,而n(MOH)=0.0025mol,说明HA过量,但溶液呈中性,说明HA为弱酸,如二者恰好反应,应生成强碱弱酸盐,促进水的电离;
(3)结合电荷守恒和物料守恒解答;
(4)HA电离出的c(H+)为0.1mol/L×0.1%=10-4mol/L,则pH=-lgc(H+)进行计算.
解答 解:(1)由图象可知0.1mol/L MOH溶液的pH=13,c(OH-)=0.1mol/L,说明为强碱,完全电离,则电离方程式为:MOH═M++OH-,
故答案为:MOH═M++OH-;
(2)由图象可知,当加入13mL 0.2mol/L HA溶液时,n(HA)=0.0026mol,而n(MOH)=0.0025mol,说明HA过量,但溶液呈中性,说明HA为弱酸,如二者恰好反应,应生成强碱弱酸盐,水解呈碱性,发生A-+H2O?HA+OH-,促进水的电离,则混合溶液中由水电离出的c(H+)大于0.2mol/L HA溶液中由水电离出的c(H+),
故答案为:碱;A-+H2O?HA+OH-;>;
(3)D点时,加入n(HA)=0.005mol,而加入n(MOH)=0.0025mol,A元素以A-和HA两种形式存在,而M全以M+形式存在,溶液中c(A-)+c(HA)=2c(M+);
c(M+)=0.05mol/L,c(OH-)=1×10-11mol/L,由电荷守恒c(M+)+c(H+)=c(A-)+c(OH-)和物料守恒c(A-)+c(HA)=2c(M+)可得:c(HA)+c(H+)=c(M+)+c(OH-)=0.05mol/L+10-11mol/L,
故答案为:=;0.05+10-11;
(4)HA电离出的c(H+)为:0.1mol/L×0.1%=10-4mol/L,则pH=-lg(10-4)=4,
故答案为:4.
点评 本题考查了酸碱混合溶液定性判断,题目难度中等,试题侧重于学生的分析能力的考查,为高考常见题型,明确图象中各个点的含义是解本题关键,结合电荷守恒、物料守恒来分析解答,注意溶液的导电能力与离子浓度的关系.

 阅读快车系列答案
阅读快车系列答案| A. | C | B. | N | C. | Si | D. | P |
| A. |  | B. | C2H2 | C. |  | D. | 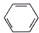 |
| A. | 甲酸、乙醛、乙酸 | B. | 苯、苯酚、己烯 | ||
| C. | 乙醇、四氯化碳、乙酸乙酯 | D. | 苯、甲苯、环己烷 |
①工业“三废”未经处理直接排放 ②植树造林,加大绿化面积 ③随意丢弃废旧电池和塑料制品垃圾 ④生活污水的任意排放 ⑤减少空气中硫氧化物和氮氧化物的排放,防止生成酸雨.
| A. | ①④⑤ | B. | ②④⑤ | C. | ①②⑤ | D. | ①③④ |
| A. | 机动车安装尾气净化器 | |
| B. | 改变用燃烧方式使植物变肥料的方法 | |
| C. | 开发新能源,减少化石燃料的使用 | |
| D. | 提议将所有发电厂、化工厂搬迁到郊区 |
| A. |  | B. | CH2=CH-CH=CH2 | C. |  | D. |  |
| A. | 石油破裂的主要目的是得到乙烯 | |
| B. | 有机物结构的分析方法有核磁共振法、红外光谱法、质谱法和紫外光谱法等 | |
| C. | 李比希提出基团的概念,并首次使用无机盐合成尿素,突破了有机物与无机物的界限 | |
| D. | 糖类、油脂、蛋白质是人类重要营养物质 |
 ,形成该化合物的化学键有离子键和共价键
,形成该化合物的化学键有离子键和共价键