题目内容
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g),经2min后,测得D的浓度为0.5molL-1,c(A):c(B)=3:4,C的平均反应速率为0.5molL-1min-1。下列说法不正确的是
A.2min后,测得A的转化率为33.3%
B.反应开始前容器中的A、B的物质的量各为4.5mol
C.2min内,用B表示的化学反应速率ν(B)=0.25molL-1min-1
D.x的值为4
【答案】C
【解析】
将等物质的量的A、B混合于2L的密闭容器中,经5min后,测得D的浓度为0.5mol/L,生成的D为2L×0.5mol/L=1mol,则:
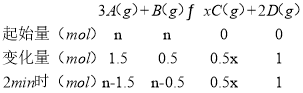
由于2min时c(A):c(B)=3:4,则(n-1.5):(n-0.5)=3:4,解得n=4.5,C的平均反应速率为0.5mol/(Lmin),则生成C的物质的量为0.5mol/(Lmin)×2L×2min=2mol,则n(C):n(D)=0.5x:1=2:1,x=4,据此分析解题;
将等物质的量的A、B混合于2L的密闭容器中,经5min后,测得D的浓度为0.5mol/L,生成的D为2L×0.5mol/L=1mol,则:
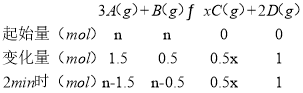
由于2min时c(A):c(B)=3:4,则(n-1.5):(n-0.5)=3:4,解得n=4.5,C的平均反应速率为0.5mol/(Lmin),则生成C的物质的量为0.5mol/(Lmin)×2L×2min=2mol,则n(C):n(D)=0.5x:1=2:1,x=4;
A.2min后,测得A的转化率为![]() =33.3%,故A正确;
=33.3%,故A正确;
B.由分析知n=4.5,即反应开始前容器中的A、B的物质的量各为4.5mol,故B正确;
C.2min内,用B表示的化学反应速率ν(B)= =0.125molL-1min-1,故C错误;
=0.125molL-1min-1,故C错误;
D.由分析知x=4,故D正确;
故答案为C。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
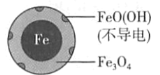
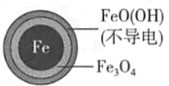
(1)Fe还原水体中NO3-的反应原理如图所示。

①作负极的物质是____。
②正极的电极反应式是____。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。