��Ŀ����
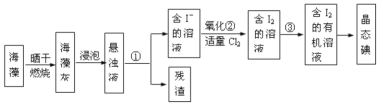
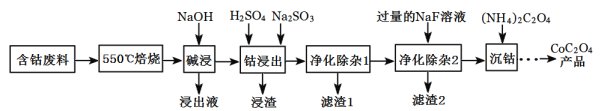
����Ŀ��CoC2O4���Ʊ������ܵ�ԭ�ϡ����ú��ܷ���(��Ҫ�ɷ�ΪCo2O3��������Fe2O3��Al2O3��CaO��MgO��̼���л����)��ȡCoC2O4�Ĺ���������ͼ��
(1)��550����������Ŀ����_______��
(2)������Һ������Ҫ�ɷ���_______��
(3)���ܽ�����������Co3+ת��ΪCo2+����Ӧ�����ӷ���ʽΪ_________��
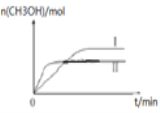
(4)����������1�������У�����40��50������H2O2��Һ����Ŀ����______��(�����ӷ���ʽ��ʾ)����������80��85��������Na2CO3��Һ����pH��5��������I������Ҫ�ɷ���______��
(5)����������2���ɽ��ơ�þ����ת��Ϊ�������˳�ȥ����������Һ��c(Ca2+)=1.0��l0-5mol/L������Һ��c(Mg2+)Ϊ___[��֪Ksp(MgF2)=7.35��10-11��Ksp(CaF2)=1.05��10-10]
(6)Ϊ�ⶨ�Ƶõ�CoC2O4��Ʒ�Ĵ��ȣ��ֳ�ȡ1.000g��Ʒ���������ʵ��Լ�ת��Ϊ�����[(NH4)2C2O4]��Һ�����ù���ϡ�����ữ����0.1000mol/L���������Һ�ζ����ﵽ�ζ��յ㣬����ȥ���������Һ26.00mL���ò�Ʒ�Ĵ���Ϊ_______________��
���𰸡���ȥ̼���л��� NaAlO2 2Co3++SO32-+H2O=2Co2++SO42-+2H+ 2Fe2++2H++H2O2=2Fe3++2H2O Fe(OH)3 7.0��10-6mol/L 95.55%
��������
���ú��ܷ���(��Ҫ�ɷ�ΪCo2O3��������Fe2O3��Al2O3��CaO��MgO��̼���л����)��ȡCoC2O4����Ҫ��̼���л�����550�����ճ�ȥ������NaOH��Al2O3�ܽ�ת��ΪNaAlO2�������Һ�����û�ԭ��Na2SO3��Co3+��ԭΪCo2+��ͬʱҲ�ὫFe3+��ԭΪFe2+��������������1�������У��������������ͬʱ����pH����Fe2+ת��ΪFe3+������ת��ΪFe(OH)3������Ȼ����������NaF��Һ����Mg2+��Ca2+ת��ΪMgF2��CaF2������ȥ��������(NH4)2C2O4��Һ����Co2+ת��ΪCoC2O4��
(1)̼���л�����п�ȼ�ԣ���550����������Ŀ���dz�ȥ̼���л����Ϊ����ȥ̼���л��
(2)�����������У�ֻ��Al2O3����NaOH��Һ��������ӦAl2O3+2NaOH��2NaAlO2+H2O������������Һ������Ҫ�ɷ���NaAlO2����Ϊ��NaAlO2��
(3)���ܽ�����������Co3+ת��ΪCo2+��ͬʱNa2SO3ת��ΪNa2SO4����Ӧ�����ӷ���ʽΪ2Co3++SO32-+H2O=2Co2++SO42-+2H+����Ϊ��2Co3++SO32-+H2O=2Co2++SO42-+2H+��
(4)����������1�������У��������������ͬʱ����pH����Fe2+ת��ΪFe3+������ת��ΪFe(OH)3���������ԣ���40��50������H2O2��Һ����Ŀ����2Fe2++2H++H2O2=2Fe3++2H2O����������80��85��������Na2CO3��Һ����pH��5��ʹ������ת��Ϊ������������������������I������Ҫ�ɷ���Fe(OH)3����Ϊ��2Fe2++2H++H2O2=2Fe3++2H2O��Fe(OH)3��
(5)����������2���ɽ��ơ�þ����ת��Ϊ�������˳�ȥ����������Һ��c(Ca2+)=1.0��l0-5mol/L������Һ��c(Mg2+)=![]() =
= ![]() mol/L=7.0��10-6mol/L������7.0��10-6mol/L��
mol/L=7.0��10-6mol/L������7.0��10-6mol/L��
(6)KMnO4��H2C2O4��Ӧ�Ĺ�ϵʽΪ��2KMnO4����5H2C2O4��n(CoC2O4)= n(H2C2O4)=![]() ��0.1000mol/L��0.02600L=0.0065mol���ò�Ʒ�Ĵ���Ϊ
��0.1000mol/L��0.02600L=0.0065mol���ò�Ʒ�Ĵ���Ϊ![]() =95.55%����Ϊ��95.55%��
=95.55%������95.55%��

����Ŀ���ƺͼ��Ǽ����õĽ���Ԫ�أ��ƺͼؼ����������������������й㷺��Ӧ�á�
��1��д�����ֿ���ʳ�õĺ��ƻ�����Ļ�ѧʽ��________����0.01 mol��������(��Na2O2����Na2O����Na2CO3����NaCl)�ֱ����100 mL����ˮ�У��ָ������£�������Һ��������Ũ���ɴ�С��˳����(��Һ����仯���Բ���)_______��
��2�����ڼر��Ƹ����ã��Ʊ�K2Oһ�����õ��ʼػ�ԭ��Ӧ�Ĺ�����������λ��������Σ���д���ü�������ط�Ӧ��ȡK2O�Ļ�ѧ����ʽ(����һ�ֵ�������)��______________________��K2O2Ҳ��ǿ�����ԣ���д������SO2������Ӧ�Ļ�ѧ����ʽ��_______________________��
��3��ijѧ����Na2CO3�� KHCO3��ɵ�ij��������ʵ�飬����������(��������ʵ���Ũ������Ҳ�����HCl�Ļӷ�)
ʵ����� | �� | �� | �� | �� |
�������/mL | 50 | 50 | 50 | 50 |
��������/g | 3.06 | 6.12 | 9.18 | 12.24 |
�����������/L(���) | 0.672 | 1.344 | 1.568 | 1.344 |
�������ݼ���������������ʵ���Ũ��Ϊ__________��ԭ�������Ʒ��n(Na2CO3)��n(KHCO3)��_________��