题目内容
【题目】下列有关实验装置的说法中正确的是( )

A.用图1装置可以实现化学能持续转化为电能
B.放出图2装置中全部液体,体积为42.00 mL
C.用图3装置可以制备少量氢氧化铁胶体
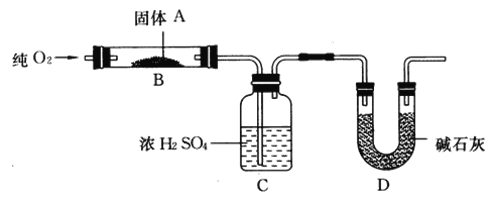
D.用图4装置可以检验乙醇脱水后有乙烯生成
【答案】C
【解析】
A.要实现化学能持续转化为电能,应该把Zn电极放入ZnCl2溶液中,把石墨电极放入盐酸中,A错误;
B.图示的仪器小刻度在下,大刻度在上,表示的是量筒,精确度是0.1 mL,不能精确到0.01 mL,因此放出图2装置中全部液体,体积为42.0 mL,B错误;
C.氢氧化铁胶体的制取方法是:向沸腾的蒸馏水中滴加几滴饱和氯化铁饱和溶液,继续加热液体呈红褐色,停止加热,得到的红褐色液体就是氢氧化铁胶体,C正确 ;
D.乙醇易挥发,乙醇能被酸性高锰酸钾溶液氧化而使溶液褪色,同时乙醇与浓硫酸发生氧化还原反应生成的二氧化硫也能使酸性高锰酸钾溶液褪色,因此不能确定是否产生了乙烯,D错误;
故合理选项是C。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】已知:在室温下有以下平衡:
编号 | 平衡方程式 | 平衡常数 |
① | HCNH++CN- | Ka=1×10-10 |
② | H2OH++OH- | Kw=1×10-14 |
③ | CN-+H2OHCN+OH- | K=? |
则下列判断错误的是
A.①的ΔS>0, ΔH>0
B.用标准NaOH溶液滴定浓度约为0.01molL-1HCN,可用甲基橙做指示剂
C.0.2molL-1的HCN溶液中加入等体积的0.1molL-1NaOH溶液,则该溶液呈碱性
D.0.2molL-1的HCN溶液中加入等体积的0.1molL-1NaOH所得的混合溶液中:2c(H+)+c(HCN)=2c(OH-)+c(CN-)
【题目】(I)已知在448 ℃时,反应H2(g)+I2(g)![]() 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)![]() H2(g)+I2(g)的平衡常数K2为______;反应
H2(g)+I2(g)的平衡常数K2为______;反应![]() H2(g)+
H2(g)+![]() I2(g)
I2(g)![]() HI(g)的平衡常数K3为________。
HI(g)的平衡常数K3为________。
(II)在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____。
(2)该反应为_____(填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____℃。
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol·L1,c(H2)=1.5mol·L1,c(CO)=1mol·L1,c(H2O)=3mol·L1,则下一时刻,反应向_____(填“正向”或“逆向”)进行。