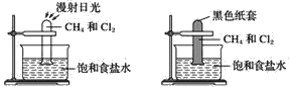
题目内容
【题目】(I)已知在448 ℃时,反应H2(g)+I2(g)![]() 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)![]() H2(g)+I2(g)的平衡常数K2为______;反应
H2(g)+I2(g)的平衡常数K2为______;反应![]() H2(g)+
H2(g)+![]() I2(g)
I2(g)![]() HI(g)的平衡常数K3为________。
HI(g)的平衡常数K3为________。
(II)在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____。
(2)该反应为_____(填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____℃。
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol·L1,c(H2)=1.5mol·L1,c(CO)=1mol·L1,c(H2O)=3mol·L1,则下一时刻,反应向_____(填“正向”或“逆向”)进行。
【答案】![]() 7
7 ![]() 吸热 830 逆向
吸热 830 逆向
【解析】
(I)先写出三个反应的化学平衡常数表达式,然后对比,找出平衡常数的关系,从而可得K2、K3的数值;
(II)(1)根据平衡常数的含义书写该反应的平衡常数表达式;
(2)根据温度对平衡常数的影响,结合温度与平衡移动原理的关系判断;
(3)将该平衡浓度关系变形,计算平衡常数的值,再与表格数据对照,得到反应温度;
(4)将相应物质的浓度带入浓度商式中,计算其数值,再与该温度下的平衡常数进行比较,判断反应进行的方向。
(I)反应H2(g)+I2(g)![]() 2HI(g)的平衡常数K1为49,K1=
2HI(g)的平衡常数K1为49,K1=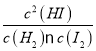 =49,该温度下反应2HI(g)
=49,该温度下反应2HI(g)![]() H2(g)+I2(g)的平衡常数K2=
H2(g)+I2(g)的平衡常数K2=![]() =
=![]() ;反应
;反应![]() H2(g)+
H2(g)+![]() I2(g)
I2(g)![]() HI(g)的平衡常数K3=
HI(g)的平衡常数K3=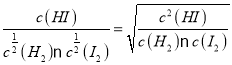 =
=![]() =7;
=7;
(II)(1)由于化学平衡常数是可逆反应达到平衡状态时各种生成物浓度幂之积与各种反应物浓度幂之积的比,所以化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)的化学平衡常数K=
CO(g)+H2O(g)的化学平衡常数K=![]() ;
;
(2)根据表格数据可知:温度升高,化学平衡常数增大,说明升高温度,平衡正向移动,根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,所以该反应的正反应为吸热反应;
(3)将该平衡浓度关系c(CO2)·c(H2)=c(CO)·c(H2O)变形,![]() = 1,可得其平衡常数的值为1,由表格中温度与化学平衡常数的数据关系可知反应温度是830℃;
= 1,可得其平衡常数的值为1,由表格中温度与化学平衡常数的数据关系可知反应温度是830℃;
(4)该反应在某时刻的浓度商数值为Qc=![]() =1,数值大于800℃的化学平衡常数0.9,说明生成物的浓度相对较大,因此下一时刻反应逆向进行。
=1,数值大于800℃的化学平衡常数0.9,说明生成物的浓度相对较大,因此下一时刻反应逆向进行。

【题目】在密闭容器中发生:![]() ,已知:c(CO2)随温度(T)、时间(t)的变化曲线如图所示,则:
,已知:c(CO2)随温度(T)、时间(t)的变化曲线如图所示,则:
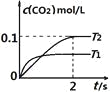
(1)T1____________T2 , 其理由是____________
(2)在T2温度下,0~2s内的平均反应速率v(N2)=____________
(3)下列叙述中能判断该反应达平衡状态的是____________
A. 平衡体系中气体压强不再改变 B. 平衡体系中气体密度不再改变
C. c(CO2):c(N2)=2:1 D. V正(CO):V逆(N2)=2:1
(4)若容器恒容,绝热,加热使容器内温度迅速升至原来的2倍,达到新平衡后,容器内温度________(填“大于”“小于”或“等于”)原来的2倍。
(5)在温度T3下,在两个体积均为1.0L的恒容密闭容器中发生该反应.
容器编号 | 起始物质的量 | 平衡时物质的量 |
Ⅰ | 2.0molNO,2.0molCO | 1.0molCO2 |
Ⅱ | 4.0molNO,4.0molCO |
①T3时该反应的平衡常数K=_________,若起始时向容器Ⅰ中充入1.0mol NO,1.5mol CO和2.0molCO2, 0.5molN2, 则反应向_________(填“正”或“逆”)反应方向进行。
②平衡时两容器中CO的转化率:Ⅰ_________Ⅱ,容器Ⅰ中反应达平衡后,若要进一步提高CO的转化率,可采取的措施为(请写出两条)_________________ __________________。