题目内容
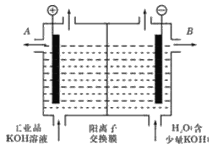
【题目】某废水含Na+、K+、Mg2+、Cl-和SO42-等离子。利用微生物电池进行废水脱盐的同时处理含OCN-的酸性废水,装置如图所示。下列说法错误的是
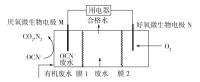
A.好氧微生物电极N为正极
B.膜1、膜2依次为阴离子、阳离子交换膜
C.通过膜1和膜2的阴离子总数一定等于阳离子总数
D.电极M的电极反应式为2OCN-6e+2H2O=2CO2↑+N2↑+4H
【答案】C
【解析】
A.由物质转化知,OCN中C为+4价,N为-3价,在M极上N的化合价升高,说明M极为负极,N极为正极,A项正确;
B.在处理过程中,M极附近电解质溶液正电荷增多,所以阴离子向M极迁移,膜1为阴离子交换膜,N极反应式为O2+4e+2H2O=4OH,N极附近负电荷增多,阳离子向N极迁移,膜2为阳离子交换膜,B项正确;
C.根据电荷守恒知,迁移的阴离子、阳离子所带负电荷总数等于正电荷总数,但是离子所带电荷不相同,故迁移的阴、阳离子总数不一定相等,C项错误;
D.M极发生氧化反应,水参与反应,生成了H,D项正确;
答案选C。

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目