题目内容
【题目】金属铝在生产生活中有着广泛的用途。回答下列问题:
(1)铝元素在周期表中的位置是_______________。
(2)比较原子结构示意图:它们的共同之处是___________![]() 选填编号,下同
选填编号,下同![]() ;不同之处是___________。
;不同之处是___________。
a.电子层数b.次外层电子数c.最外层电子数d.质子数
(3)常温下铝制容器可以用来盛放浓硫酸而不被溶解,这种现象称为___________。
氢氧化铝和盐酸反应的化学方程式为_________________________________。
能把溶液中的铁离子和铝离子分离开的试剂是___________。![]() 选填编号
选填编号![]()
a.盐酸b.硫酸铜溶液 c.氨水 d.氢氧化钠溶液
【答案】第三周期第IIIA族 ab cd 钝化反应 Al(OH)3+3HCl=AlCl3+3H2O d
【解析】
(1)铝是13号元素,在周期表中的位置是第三周期第IIIA族;
(2) 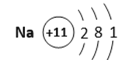 ,原子结构示意图的含义:圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示电子数。
,原子结构示意图的含义:圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示电子数。
(3)常温下铝制容器可以用来盛放浓硫酸而不被溶解,是因为在铝表面形成致密的氧化薄膜,这种现象是钝化反应;由于氢氧化铝是两性氢氧化物,故可与NaOH继续反应,而沉淀溶解,可用来分离铁离子和铝离子。
(1)铝是13号元素,在周期表中的位置是第三周期第IIIA族;
(2)从三个原子结构示意图中可看出,均有3个电子层、次外层电子数均为8,故相同的之处是ab;而最外层电子数均不相同、核内质子数也都不同,故不同之处是cd;
(3)常温下铝与浓硫酸反应生成氧化铝,在铝表面形成一层致密的氧化铝薄膜,阻止硫酸进一步与铝制容器反应,这种现象叫钝化反应;
氢氧化铝和盐酸反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O;
铁离子能与氢氧化钠溶液反应生成氢氧化铁沉淀,铝离子也能与氢氧化钠溶液反应生成氢氧化铝沉淀,但氢氧化铝是两性氢氧化物,可与NaOH继续反应,化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O,即铁离子转为氢氧化铁难溶物、铝离子转化为NaAlO2可溶物,则氢氧化钠溶液能分离铁离子和铁离子,答案选d。