题目内容
【题目】由硫铁矿烧渣(主要成分:Fe2O3、Al2O3、FeO、SiO2)制备绿矾(FeSO47H2O)的流程如下:

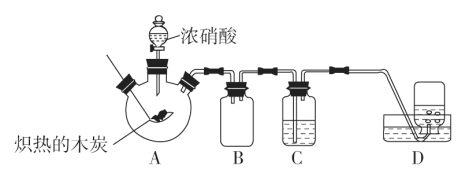
已知:①FeS2难溶于水,能还原Fe3+,硫元素被氧化成SO42-。
②金属离子生成氢氧化物沉淀的pH范围见下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.5 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 6.3 | 8.3 |
(1)滤渣Ⅰ的主要成分可与某种酸反应,其气态产物的电子式为____________;滤渣Ⅱ经灼烧后可用于_______(写出一种用途即可)。
(2)“还原”的目的是__________,写出“还原”步骤中涉及反应的离子方程式_________。
(3)“除铝”反应过程中控制的pH范围是_______________________。
(4)操作Ⅲ包含3个基本的实验操作,依次是_______________,“洗涤”时的试剂最好选用下列中的____________(填代号)
A.热水 B.氯水 C.乙醇 D.饱和食盐水
(5)设计实验检验制得的绿矾晶体中是否含有Fe3+:___________________________。
【答案】![]() 冶炼制取铝(或作耐火材料等) 将Fe3+还原为Fe2+后,便于分离铁元素和铝元素 FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+ 大于或等于5.0,且小于6.3(或5.0≤pH<6.3) 蒸发浓缩、冷却结晶、过滤 C 取少量样品加水溶解配成溶液,滴加KSCN溶液,若溶液不变红色,说明无Fe3+;若溶液呈红色,说明其中含有Fe3+
冶炼制取铝(或作耐火材料等) 将Fe3+还原为Fe2+后,便于分离铁元素和铝元素 FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+ 大于或等于5.0,且小于6.3(或5.0≤pH<6.3) 蒸发浓缩、冷却结晶、过滤 C 取少量样品加水溶解配成溶液,滴加KSCN溶液,若溶液不变红色,说明无Fe3+;若溶液呈红色,说明其中含有Fe3+
【解析】
硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3)中加入稀硫酸,得到:Fe2+、Fe3+、Al3+的酸性溶液,二氧化硅不反应,过滤,滤渣Ⅰ为二氧化硅,在滤液中加入FeS2,将Fe3+还原为Fe2+,反应为:FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+,调节溶液pH,生成氢氧化铝沉淀,滤渣Ⅱ为氢氧化铝,滤液为硫酸亚铁溶液,用稀硫酸酸化硫酸亚铁溶液后,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得到FeSO47H2O,以此解答该题。
(1)分析知滤渣Ⅰ为SiO2,是酸性氧化物,但能溶于HF生成SiF4,气态产物SiF4是共价化合物,其电子式为![]() ;滤渣Ⅱ为Al(OH)3,受热分解的产物为Al2O3,因其高熔点,作耐火材料,也可通过电解冶炼得到Al;
;滤渣Ⅱ为Al(OH)3,受热分解的产物为Al2O3,因其高熔点,作耐火材料,也可通过电解冶炼得到Al;
(2) 利用FeS2可将Fe3+还原为Fe2+,同时生成SO42-,结合守恒法可知发生反应的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+;
(3)“除铝”的目的是使溶液中Al3+完全沉淀,而溶液中的Fe2+不沉淀,则结合金属离子生成氢氧化物沉淀的pH范围表中数据,可知控制的pH范围是5.0≤pH<6.3;
(4)从硫酸亚铁溶液中获取绿矾晶体,需要经过蒸发浓缩、冷却结晶、过滤3个基本操作,其中“洗涤”时为减小绿矾晶体的溶解不使用热水,而选择乙醇,另外氯水能氧化Fe2+,也不宜用来洗涤绿矾,而饱和食盐水洗涤时绿矾表面会附杂质离子,而不纯,故只能选择乙醇洗涤,答案为C;
(5)利用含有Fe3+的溶液中滴加KSCN溶液会变红色,则检验制得的绿矾晶体中是否含有Fe3+的操作方法是将绿矾样品溶于水,取少量于试管中,滴加KSCN溶液,若溶液变成红色,说明含Fe3+,若溶液不变色,则不含Fe3+。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
实验方案 | 实验现象 |
①用砂纸擦后的镁带与沸水反应,再向反应液中滴加酚酞 | A.浮于水面,熔成小球,在水面上无定向移动,随之消失,溶液变成红色 |
②向新制的H2S饱和溶液中滴加新制的氯水 | B.产生大量气体,可在空气中燃烧,溶液变成浅红色 |
③钠与滴有酚酞试液的冷水反应 | C.反应不十分强烈,产生的气体可以在空气中燃烧 |
④镁带与2mol·L-1的盐酸反应 | D.剧烈反应,产生的气体可以在空气中燃烧 |
⑤铝条与2mol·L-1的盐酸反应 | E.生成白色胶状沉淀,继而沉淀消失 |
⑥向氯化铝溶液中滴加氢氧化钠溶液 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:______________________________________。
(2)实验用品:仪器___________________等;药品________________________等。
(3)实验内容:(*填写题给信息表中的序号)
实验方案* | 实验现象* | 有关化学方程式 |
_______________________________
(4)实验结论:______________________________________。
(5)请从结构理论上简单说明具有上述结论的原因___________________。
(6)请你补充一组实验方案(简单易行),证明此周期中另外两种元素的性质递变规律_____________________________________。