题目内容
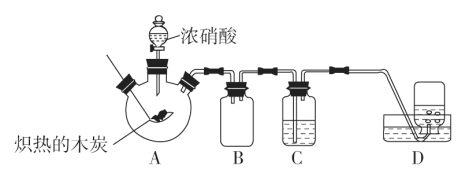
【题目】某化学学习小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO3![]() 4NO2↑+O2↑+2H2O)。
4NO2↑+O2↑+2H2O)。
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入三口烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三口烧瓶中产生的气体颜色为__,产生该现象的化学方程式是__。
(2)装置C中盛有足量澄清石灰水,炽热的木炭与浓硝酸反应后可观察到C中的现象是__。
(3)装置B的作用是__。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。
①下列对该气体的检验方法合适的是__。
A.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
B.敞口观察装置D中集气瓶内气体的颜色变化
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶中收集的无色气体是氧气,则氧气的来源是__。
【答案】红棕色 C+4HNO3(浓)![]() 4NO2↑+CO2↑+2H2O 澄清石灰水变浑浊 防倒吸 BC 浓硝酸的分解
4NO2↑+CO2↑+2H2O 澄清石灰水变浑浊 防倒吸 BC 浓硝酸的分解
【解析】
本实验的目的是探究浓硝酸与木炭的反应,连接装置,检查装置的气密性,然后装药品,实验开始,装置A中进行碳单质和浓硝酸加热反应,浓硝酸具有强氧化性可以将碳单质氧化成成二氧化碳,反应的化学方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,根据题意可知同时有副反应副反应:4HNO3
CO2↑+4NO2↑+2H2O,根据题意可知同时有副反应副反应:4HNO3![]() 4NO2↑+O2↑+2H2O;装置B作为安全瓶,可以防倒吸,装置C中盛有足量澄清石灰水溶液,可以检验并吸收二氧化碳,装置D收集尾气。
4NO2↑+O2↑+2H2O;装置B作为安全瓶,可以防倒吸,装置C中盛有足量澄清石灰水溶液,可以检验并吸收二氧化碳,装置D收集尾气。
(1)反应过程中有二氧化氮气体生成,二氧化氮为红棕色,所以可以观察到三口烧瓶中产生的气体颜色为红棕色;化学方程式为C+4HNO3(浓)![]() 4NO2↑+CO2↑+2H2O;
4NO2↑+CO2↑+2H2O;
(2)木炭与浓硝酸反应会生成二氧化碳,从而使澄清石灰水变浑浊;
(3)装置B为安全瓶,可以防止倒吸;
(4)①A.一氧化氮不溶于水,与水不反应,湿润的蓝色石蕊试纸不能区别一氧化氮和氧气,故A检验方法不合适;
B.一氧化氮和氧气反应生成二氧化氮,二氧化氮为红棕色,如果集气瓶内气体是NO,向装置D中通入O2,可以看到红棕色,故B检验方法合适;
C.将带火星的木条伸入集气瓶中,若为氧气则木条复燃,故C检验方法合适;
综上所述答案为BC;
②根据题意可知浓硝酸在加热条件下可以分解产生氧气。

 初中暑期衔接系列答案
初中暑期衔接系列答案【题目】由硫铁矿烧渣(主要成分:Fe2O3、Al2O3、FeO、SiO2)制备绿矾(FeSO47H2O)的流程如下:

已知:①FeS2难溶于水,能还原Fe3+,硫元素被氧化成SO42-。
②金属离子生成氢氧化物沉淀的pH范围见下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.5 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 6.3 | 8.3 |
(1)滤渣Ⅰ的主要成分可与某种酸反应,其气态产物的电子式为____________;滤渣Ⅱ经灼烧后可用于_______(写出一种用途即可)。
(2)“还原”的目的是__________,写出“还原”步骤中涉及反应的离子方程式_________。
(3)“除铝”反应过程中控制的pH范围是_______________________。
(4)操作Ⅲ包含3个基本的实验操作,依次是_______________,“洗涤”时的试剂最好选用下列中的____________(填代号)
A.热水 B.氯水 C.乙醇 D.饱和食盐水
(5)设计实验检验制得的绿矾晶体中是否含有Fe3+:___________________________。