题目内容
12.镁粉是制造烟花的重要原料之一,生产镁粉时,将镁蒸气在某种气体中冷却,下列气可作为冷却气的是( )| A. | 空气 | B. | 氮气 | C. | 氩气 | D. | 二氧化碳 |
分析 Mg可与空气中氧气反应生成MgO、可与N2反应生成Mg3N2、可在CO2中燃烧生成MgO,而稀有气体氩气不与镁反应,以此来解答.
解答 解:空气中的氧气、氮气、二氧化碳均与Mg反应,不能作为冷却气,只有氩气不与镁反应,可作为冷却气,
故选C.
点评 本题考查Mg的化学性质,为高频考点,把握物质的性质及发生的反应为解答的关键,注意性质与用途的关系,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
2.将5.6g铁粉投入盛有200mL 含0.1mol硫酸的烧杯中,2min 时铁粉刚好溶解完全.如果反应前后溶液的体积不变,则该反应的平均速率可表示为( )
| A. | v(Fe)=0.5 mol•L-1•min-1 | B. | v(H2SO4)=1 mol•L-1•min-1 | ||
| C. | v(H2)=0.25 mol•L-1•min-1 | D. | v(FeSO4)=0.25 mol•L-1•min-1 |
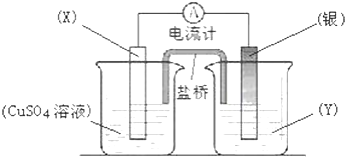
20.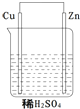 关于如图所示的原电池下列叙述正确的是( )
关于如图所示的原电池下列叙述正确的是( )
①电子由铜流向锌
②正极反应式为Cu+2e-=Cu2+
③SO42-向铜极移动
④铜电极上有气泡
⑤若有0.5mole-流经导线,则可产生0.25molH2
⑥烧杯中溶液的PH升高.
 关于如图所示的原电池下列叙述正确的是( )
关于如图所示的原电池下列叙述正确的是( )①电子由铜流向锌
②正极反应式为Cu+2e-=Cu2+
③SO42-向铜极移动
④铜电极上有气泡
⑤若有0.5mole-流经导线,则可产生0.25molH2
⑥烧杯中溶液的PH升高.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③⑤ | D. | ②④⑥ |
17.橙花醇具有玫瑰及苹果香气,可作为香料,其结构简式如下:

下列关于橙花醇的叙述,错误的是( )

下列关于橙花醇的叙述,错误的是( )
| A. | 既能发生取代反应,也能发生加成反应 | |
| B. | 在浓硫酸催化下加热脱水,可以生成不止一种四烯烃 | |
| C. | 1mol橙花醇与浓氢溴酸反应,最多消耗3mol HBr | |
| D. | 1mol橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗 480g Br2 |
4.某恒温密闭容器中,可逆反应A(s)?B(?)+C(g)△H=+a kJ/mol达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内c(A)消耗﹕c(C)消耗=1﹕1 | |
| C. | 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 | |
| D. | 若开始时向容器中加入1molB和1molC,达到平衡时放出热量a kJ |
1.化学与生产、生活、社会密切相关,下列说法正确的是( )
| A. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| B. | 煤燃烧时加入少量的生石灰可以减少废气中二氧化硫排放 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 聚氟乙烯是纯净物 |
2.设NA为阿伏加德罗常数的数值.下列说法错误的是( )
| A. | 1mol NH3中含有3NA个N-H键 | |
| B. | 36g C60含分子数为0.05NA | |
| C. | 标准状况下,11.2L CO2中含有2NA个共用电子对 | |
| D. | 18g重水(${\;}_{1}^{2}$H2O)中含有10NA个电子 |