��Ŀ����
����Ŀ��ij�о�С��ͬѧΪ̽��п�����ᷴӦ����SO2��H2���ٽ�Ũ��(Ũ��������п��Ӧ����SO2�����Ũ��)���������ʵ�顣�ڴ��Թ�A�м���100mL 18mol/L���ᣬ�����������ϰ��ϵĶ���������ڼ���������п��(���ϰ����������ƶ�)�����Լ�ƿD�м���������ŨNaOH��Һ(���Ⱥͼг�װ����ʡ��)��
��֪��п��Ũ����Ӵ�����ʼʱ��Ӧ�����������ʵ������Լ����䷴Ӧ�����д�����������ʱ���÷�Ӧ���ʻ����Լӿ첢���д������ȷų���
(1)��д��п�����ᷴӦ����SO2�Ļ�ѧ����ʽ_______��
(2)����װ����֮�����Լ�֮ǰ������еIJ�����__________��
(3)������B��������______�����û�������ƣ����ղⶨ���ٽ�Ũ�Ȼ�_______��(����ƫ��������ƫ����������Ӱ����)
(4)װ���и����C��������_______��
(5)��Ӧ��������Dװ���м���������H2O2��Һ��������BaCl2��Һ����ַ�Ӧ�����ó������ˡ�ϴ�ӡ���������õ���������Ϊa�ˣ���Ũ������п��Ӧ���ٽ�Ũ��Ϊ��_________mol/L��(�ú�a�ļ���ʽ��ʾ����������仯)
(6)ijͬѧͨ����ϵ������ԭ��Ӧ�����֪ʶ����ΪҲ�������������ữ�ĸ��������Һ��D�е�SO![]() ���еζ���ͨ���ζ�����SO
���еζ���ͨ���ζ�����SO![]() �����ʵ��������ٽ�Ũ�ȣ�����Ϊ������һ�뷨�Ƿ����?______(����������������������)��ԭ����_____��
�����ʵ��������ٽ�Ũ�ȣ�����Ϊ������һ�뷨�Ƿ����?______(����������������������)��ԭ����_____��
���𰸡�Zn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O ����װ�������� �������������� ƫ�� ������ 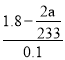 ������ ʵ������в��ܱ�֤�õ���Na2SO3��Һ�Ƿ�ᱻ�����е������������ʣ���ɵζ������ȷ
������ ʵ������в��ܱ�֤�õ���Na2SO3��Һ�Ƿ�ᱻ�����е������������ʣ���ɵζ������ȷ
��������
��ʵ���Ŀ����̽��п�����ᷴӦ����SO2��H2���ٽ�Ũ��(Ũ��������п��Ӧ����SO2�����Ũ��)��Ũ��������Zn��Ӧ�����У��ȱ���SԪ�ص������ԣ���ʱ�Ļ�ԭ����ΪSO2��֮�������ϡ��Ӧ����H2�������ɵ�SO2��װ��D����������NaOH��Һ���գ�Ȼ����Dװ���м���������H2O2��Һ��SԪ��ȫ������ΪSO![]() ��֮������������Ȼ�����Һ�õ�BaSO4������ͨ���ⶨ���ᱵ����������ȷ����Zn��Ӧ����SO2���ĵ�����������Ӷ�ȷ��ʣ�������Ũ�ȣ����ٽ�Ũ�ȡ�
��֮������������Ȼ�����Һ�õ�BaSO4������ͨ���ⶨ���ᱵ����������ȷ����Zn��Ӧ����SO2���ĵ�����������Ӷ�ȷ��ʣ�������Ũ�ȣ����ٽ�Ũ�ȡ�
(1)���ݵ����غ��Ԫ���غ�ɵ�п��Ũ���ᷴӦ����SO2�Ļ�ѧ����ʽΪZn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O��
(2)����װ����֮�����Լ�֮ǰ������еIJ����Ǽ���װ�õ������ԣ���ֹ©����
(3)��Ӧ�����лᷢ���������ȣ����ˮ�Ļӷ���ʹ�����Ũ��������п��Ӧ���ɶ������������ƫ�࣬��ɲⶨ���ٽ�Ũ��ƫС��������Ҫ�����ܵ���ͬʱ��������ˮ������
(4)��������������NaOH��Һ��������Ҫװ��C����ֹ������
(5)�õ��ij���ΪBaSO4��n(SO2)=n(BaSO4)=![]() mol�����ݷ�Ӧ����ʽ��֪��Zn��Ӧ����SO2�����ĵ���������ʵ���Ϊ
mol�����ݷ�Ӧ����ʽ��֪��Zn��Ӧ����SO2�����ĵ���������ʵ���Ϊ![]() mol��ԭŨ�������Ϊ100mL��Ũ��Ϊ18mol/L������ʣ�����������ʵ���Ϊ(1.8-
mol��ԭŨ�������Ϊ100mL��Ũ��Ϊ18mol/L������ʣ�����������ʵ���Ϊ(1.8-![]() )mol��Ũ��Ϊ
)mol��Ũ��Ϊ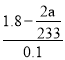 mol/L��
mol/L��
(6)ʵ������в��ܱ�֤�õ���Na2SO3��Һ�Ƿ�ᱻ�����е������������ʣ���ɵζ������ȷ�����Ը�ͬѧ���뷨�����С�

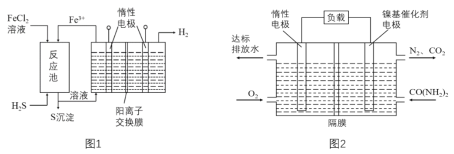
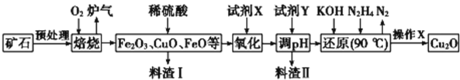
����Ŀ��������ͭ(Cu2O)��һ����;�㷺�Ĺ����ϣ�ij��������ͭ��ʯ(�� CuFeS2��Cu2S��)Ϊԭ����ȡCu2O�Ĺ����������£�
�����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±���
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
��ʼ���� | 7.5 | 2.7 | 4.8 |
��ȫ���� | 9.0 | 3.7 | 6.4 |
(1)¯���е��к�����ɷ���________��Cu2S��O2��Ӧʱ���������뻹ԭ�������ʵ���֮��Ϊ______��
(2)�Լ�X��H2O2��Һ�����Լ�X��___________ʱ���������ڽ��������ɱ���
(3)�����Լ�Y��pHʱ��pH�ĵ��ط�Χ��________��
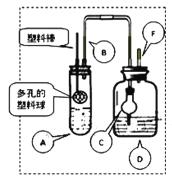
(4)����ԭ��������Ϊ���N2H4ת���ʿɲ�ȡ�Ĵ�ʩ��_________(�����)��
a�����Ͻ��裬ʹN2H4����Һ��ֽӴ� b������ͨ��N2H4������
c������KOH�Ľ����� d����Сͨ��N2H4������
(5)д����N2H4�Ʊ�Cu2O�Ļ�ѧ����ʽΪ_______________
(6)����X������ɣ����к��ʱҪ������������Ŀ����____________��