题目内容
【题目】铜与锌用导线连接后,插入稀硫酸中形成原电池。
(1)分析图并填空:__。
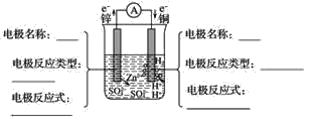
(2)原电池总反应式(离子方程式)__。
(3)上述装置产生电流的原因是__。
(4)上述装置的能量转化是__。
【答案】 Zn+2H+=Zn2++H2↑ 锌与稀硫酸发生氧化还原反应,有电子转移,负极锌失去的电子沿导线流向正极铜,闭合回路中有电流产生 化学能转化为电能
Zn+2H+=Zn2++H2↑ 锌与稀硫酸发生氧化还原反应,有电子转移,负极锌失去的电子沿导线流向正极铜,闭合回路中有电流产生 化学能转化为电能
【解析】
在铜锌原电池中,锌与稀硫酸发生氧化还原反应,有电子转移,即锌失去的电子沿导线流向铜,闭合回路中形成电流,化学能转化为电能。由于锌的活动性大于铜,锌为原电池的负极,失去电子发生氧化反应,电极反应式为Zn-2e-=Zn2+,锌片逐渐溶解;铜为原电池的正极,溶液中的氢离子在正极上得到电子发生还原反应,电极反应式为2H++2e-=H2↑,铜片表面产生大量气泡,以此解题。
在铜锌原电池中,锌与稀硫酸发生氧化还原反应,有电子转移,即锌失去的电子沿导线流向铜,闭合回路中形成电流,化学能转化为电能。由于锌的活动性大于铜,锌为原电池的负极,失去电子发生氧化反应,电极反应式为Zn-2e-=Zn2+,锌片逐渐溶解;铜为原电池的正极,溶液中的氢离子在正极上得到电子发生还原反应,电极反应式为2H++2e-=H2↑,铜片表面产生大量气泡。
(1)根据分析,该题图为: ,
,
故答案为: ;
;
(2)根据分析,由于锌的活动性大于铜,锌为原电池的负极,电极反应式为Zn-2e-=Zn2+,铜为原电池的正极,电极反应式为2H++2e-=H2↑,原电池总反应式(离子方程式) Zn+2H+=Zn2++H2↑,
故答案为:Zn+2H+=Zn2++H2↑;
(3)该装置产生电流的原因是:在铜锌原电池中,锌与稀硫酸发生氧化还原反应,有电子转移,即锌失去的电子沿导线流向铜,闭合回路中形成电流,
故答案为:锌与稀硫酸发生氧化还原反应,有电子转移,负极锌失去的电子沿导线流向正极铜,闭合回路中有电流产生。
(4)根据分析可知,该装置是原电池,原电池是将化学能转化为电能的装置,
故答案为:化学能转化为电能。

【题目】下表列出了9种元素在元素周期表中的位置示意。
周期 | ⅠA 1 | 0 18 | ||||||
1 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | ||
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | |||||
4 | ⑨ | |||||||
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_____
(2)画出元素⑧形成的简单离子的结构示意图_________________
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_________
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是__________________
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______(填化学式),写出元素⑥的单质与水反应的离子反应方程式___________________,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式__________