题目内容
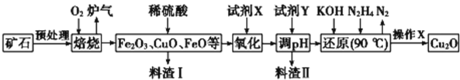
【题目】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含 CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀 | 7.5 | 2.7 | 4.8 |
完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是________,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为______。
(2)试剂X是H2O2溶液,当试剂X是___________时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是________。
(4)“还原”步骤中为提高N2H4转化率可采取的措施有_________(填序号)。
a.不断搅拌,使N2H4和溶液充分接触 b.增大通入N2H4的流速
c.减少KOH的进入量 d.减小通入N2H4的流速
(5)写出用N2H4制备Cu2O的化学方程式为_______________
(6)操作X包括烘干,其中烘干时要隔绝空气,其目的是____________。
【答案】SO2 2∶1 空气或氧气 3.7≤pH<4.8 ad 4CuSO4+N2H4+8KOH![]() 2Cu2O+N2↑+4K2SO4+6H2O 防止Cu2O被空气中氧气氧化
2Cu2O+N2↑+4K2SO4+6H2O 防止Cu2O被空气中氧气氧化
【解析】
根据流程:硫化铜矿石(含CuFeS2、Cu2S等)预处理后与氧气焙烧,根据后续流程可知该过程中Cu元素全部转化为CuO,铁元素转化为FeO和Fe2O3,根据S元素的价态规律可知其转化为SO2;加入稀硫酸溶解金属氧化物,得到含有Cu2+、Fe2+、Fe3+的酸性溶液,加入试剂X将Fe2+氧化为Fe3+,加入试剂Y调节pH为3.7~4.8沉淀Fe3+,过滤,将滤液用KOH、N2H4还原,得到氧化亚铜沉淀,过滤,洗涤、隔绝空气烘干,制得Cu2O,据此分析作答。
(1)焙烧过程中S元素会被氧化成有害气体SO2;Cu2S与O2反应时Cu元素化合价由+1价升为+2价,S元素化合价由-2价升为+4价,所以Cu2S为还原剂,整体化合价升高8价,O2为氧化剂,O元素由0价降为-2价,一个氧气降低4价,所以氧化剂和还原剂的物质的量之比为2:1;
(2)酸性条件下,氧气也可将Fe2+氧化为Fe3+,而氧气或空气价格远低于过氧化氢,故可用氧气或空气替代过氧化氢,降低成本;
(3)加入试剂Y的目的是调节pH完全沉淀Fe3+,但不沉淀Cu2+,根据表中数据可知,pH范围为:3.7≤pH<4.8;
(4)a.不断搅拌,使N2H4和溶液充分接触可以加快反应速率,提高单位时间内N2H4的转化率,故a符合题意;
b.流速过快N2H4不能充分反应,转化率减小,故b不符合题意;
c.减少KOH的进入量会降低溶液对N2H4的吸收量,转化率减小,故c不符合题意;
d.减小通入N2H4的流速可以使反应更充分,故d符合题意;
综上所述选ad;
(5)N2H4制备Cu2O的反应物有CuSO4、N2H4和KOH,产物有N2和Cu2O等,该过程中+2价的铜元素将-2价的N元素氧化,根据电子守恒和元素守恒可得化学方程式为4CuSO4+N2H4+8KOH![]() 2Cu2O+N2↑+4K2SO4+6H2O;
2Cu2O+N2↑+4K2SO4+6H2O;
(6)因为Cu2O具有还原性,在加热条件下易被空气氧化,故烘干过程要隔绝空气;

【题目】下列各组离子在溶液中可以大量共存,且加入或通入试剂X后,发生反应的离子方程式正确的是
选项 | 离子组 | 试剂X | 发生反应的离子方程式 |
A | K+、Na+、 | 少量HCl | H2O+H++ |
B |
| 少量H2S | Fe2++H2S=FeS↓+2H+ |
C | ClO-、Na+、Ca2+、 | 少量CO2 | CO2+Ca2++H2O+2ClO-=CaCO3↓+2HClO |
D | I-、Cl-、Na+、 | 少量稀硝酸 | 6I-+2 |
A.AB.BC.CD.D
【题目】下表列出了9种元素在元素周期表中的位置示意。
周期 | ⅠA 1 | 0 18 | ||||||
1 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | ||
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | |||||
4 | ⑨ | |||||||
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_____
(2)画出元素⑧形成的简单离子的结构示意图_________________
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_________
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是__________________
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______(填化学式),写出元素⑥的单质与水反应的离子反应方程式___________________,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式__________