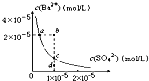��Ŀ����
����Ŀ���ϳɰ���ҵ�ڹ�ũҵ������������������Ҫ���á���Ӧԭ��Ϊ��3H2(g)+N2(g)![]() 2NH3(g) ��H < 0��
2NH3(g) ��H < 0��
��1����T ��ʱ����һ�����ʵ�����H2��N2����һ�ݻ�������ܱ������С�
�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬����__________(�����)��
a.�����ڵ�ѹǿ������ʱ��仯
b.3��(N2)=��(H2)
c��3����(H2)=2����(NH3)
d.���������ܶȱ��ֲ���
�ڴ�����ƽ��������������䣬�����¶ȣ�����___________________(��������������������������С��)�������������Ĺ�ϵΪ����___________����(���>��������������<��)����������ȡ�
�۸������´ﵽƽ��ʱ���������ڳ���������壬���������ڵ�ѹǿ��NH3�����������(�����������䡱��С��)��________
��2����T ��ʱ����һ�����ʵ�����H2��N2����һ�ݻ��ɱ���ܱ������С��ﵽƽ��ı�ijһ����ʹ��Ӧ���ʷ�������ͼ��ʾ�ı仯���ı������������______��
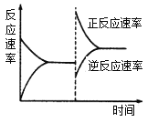
a.�����¶ȣ�ͬʱ��ѹb.�����¶ȣ�ͬʱ��ѹ
c.�����¶ȡ�ѹǿ���䣬����Ӧ��Ũ��
d.�����¶ȡ�ѹǿ���䣬��С������Ũ��
��3����T ��ʱ����0.6 mol H2��0��4 mol N2�����ݻ�Ϊ2 L���ܱ������з�����Ӧ��3H2(g)+N2(g)![]() 2NH3 (g) ��H <0���������¶Ȳ��䣬ij��ȤС��ͬѧ��÷�Ӧ������������ѹǿ��MPa����ʱ��仯��ͼ��ʾ��8 min��NH3��ƽ����������Ϊ_______��
2NH3 (g) ��H <0���������¶Ȳ��䣬ij��ȤС��ͬѧ��÷�Ӧ������������ѹǿ��MPa����ʱ��仯��ͼ��ʾ��8 min��NH3��ƽ����������Ϊ_______��

���𰸡�a ���� < ���� c 0.01 mol��L��1��min��1
��������
��1���� �ϳɰ���ӦΪ�����С�ķ��ȷ�Ӧ,����ƽ��ʱ�����������淴Ӧ�������,��ɲ�����ж�,
a. �����ڵ�ѹǿ������ʱ��仯��˵������������ʵ������䣬����ƽ��״̬����a��ȷ��
b. ����ʱ��3��(N2)=��(H2)�������жϴ���ƽ��״̬����b����
c. ����ʱ��3����(H2)=2����(NH3)������֮�Ȳ����ڻ�ѧ������֮�ȣ���c����
d. ��Ӧ�������ﶼ�����壬����ʱ�����������䣬�ܶ�Ҳ���䣬��d����
��ѡ��a��
��������ƽ��������������䣬�����¶ȣ��������������¶������ȷ����ƶ����÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������淴Ӧ�����ƶ���
�ʴ�Ϊ������<
���������´ﵽƽ��ʱ���������ڳ���������壬��Ȼѹǿ�������뷴Ӧ�����ʷ�ѹû�б仯����ƽ�ⲻ�ƶ���NH3��������������䣬
�ʴ�Ϊ������
��2��a�������¶ȣ�ͬʱ��ѹ��v����v��ͬʱ������ͼ��������
b�������¶ȣ�ͬʱ��ѹ��v����v��ͬʱ��С����ͼ��������
c�������¶ȡ�ѹǿ���䣬�������ڳ��뵪��������������Ӧ��Ũ�ȣ�v�������������������ʵ�������Ϊ����ѹǿ���䣬�������������Ũ�ȼ�С��v����С����ƽ������ʿ��ܱ�ԭƽ�����ȷ��
d�������¶ȡ�ѹǿ���䣬�������ڷ������������С������Ũ�ȣ�v����С���������������ʵ�����С��Ϊ����ѹǿ���䣬���������С����Ӧ��Ũ������v�������ݵ�Чƽ��֪ʶ֪����ƽ���������ԭƽ����ȣ���ͼ��������ѡ��c��
(3) ���¶Ⱥ����һ���������£�ѹǿ֮�ȵ������ʵ���֮�ȣ�����ƽ��ʱ���������ʵ���Ϊ0.84����0.4+0.6��mol=0.84mol������3H2(g)+N2(g)![]() 2NH3 (g)��n=2��֪�����ɵİ���Ϊ0.16mol���ٸ���v=��c��t���������Ϊ0.16mol��2L��8min=0.01 mol��L��1��min��1
2NH3 (g)��n=2��֪�����ɵİ���Ϊ0.16mol���ٸ���v=��c��t���������Ϊ0.16mol��2L��8min=0.01 mol��L��1��min��1
�ʴ�Ϊ��0.01 mol��L��1��min��1

����Ŀ����ѧ��Ӧ�����ʺ��ȶ�����������������Ҫ�����塣
(1)��֪Na2S2O3��H2SO4=Na2SO4��S����SO2��H2O����ͬѧͨ���ⶨ�÷�Ӧ����ʱ��Һ����ǵ�ʱ�䣬�о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬���ʵ������(��ȡ��Һ�����Ϊ2 mL)��
ʵ���� | �¶�/�� | c(Na2S2O3)/mol��L��1 | c(H2SO4)/mol��L��1 |
�� | 25 | 0.1 | 0.1 |
�� | 25 | 0.2 | 0.1 |
�� | 50 | 0.2 | 0.1 |
������ʵ������Һ���ȱ���ǵ���______����ʵ���ţ���ͬ����
��Ϊ̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬Ӧѡ��______��______��
(2)ij�¶��£���1 L�ܱ������У�������Ӧ��2X(g)��Y(g)![]() 2Z(g)��X�����ʵ�����ʱ��ı仯���±���
2Z(g)��X�����ʵ�����ʱ��ı仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
X�����ʵ���/mol | 0.02 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
����X��Ũ�ȱ仯��ʾ0��2 s��ƽ����ѧ��Ӧ����Ϊ______mol/(L��s)��
����3 s�Ժ�X��Ũ�Ȳ��ٸı䣬��Ӧ�ﵽ��______״̬��
����˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����______(�����)��
A��v��(X)=v��(X)
B����λʱ������2 mol X����ͬʱ��1 mol Y����
C��X��Y��Z�ķ�����֮��Ϊ2��1��2
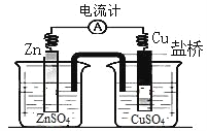
����Ŀ��Ϊ��֤��ԭ�ԣ�SO2>Fe2��>Cl��������ͬѧ�ֱ��������ͼʵ�飬������Һ1����Һ2���������ӽ����˼��飬��֤��������ԭ��˳���ʵ������(����)
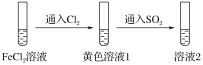
��Һ1 | ��Һ2 | |
�� | ��Fe3����Fe2�� | ��SO |
�� | ��Fe3������Fe2�� | ��SO |
�� | ��Fe3������Fe2�� | ��Fe2�� |
A.ֻ�м�B.�ס���
C.�ס���D.�ס��ҡ���
����Ŀ������˵����ȷ����
A.����������![]() �ķ�Ӧʽ
�ķ�Ӧʽ ![]()
![]()
![]()
B.���ݱ����ṩ�����ݣ������ʵ���Ũ�ȵ�NaClO��![]() �����Һ�У���
�����Һ�У���![]()
��ѧʽ | ���볣�� |
HClO |
|
|
|
|
C.�����£���![]() ��ϡ����ϡ��10�������и����ӵ����ʵ���Ũ�ȶ���Ϊԭ����ʮ��֮һ
��ϡ����ϡ��10�������и����ӵ����ʵ���Ũ�ȶ���Ϊԭ����ʮ��֮һ
D.ij�¶�ʱ��![]() ��ˮ�еij����ܽ�ƽ��������ͼ��ʾ���ܶȻ�����
��ˮ�еij����ܽ�ƽ��������ͼ��ʾ���ܶȻ�����![]() �����
�����![]() ��ʹ��Һ��a��䵽b�㣻ͨ����������ʹ��Һ��d��䵽c��
��ʹ��Һ��a��䵽b�㣻ͨ����������ʹ��Һ��d��䵽c��