��Ŀ����
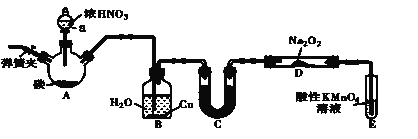
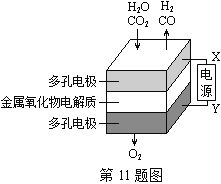
����Ŀ�����ͭ����ȼ�ϵ�أ���ͼ�������ߡ��ɱ��ͣ��õ��ͨ��һ�ָ��ӵ�ͭ��ʴ���������������������зŵ����Ϊ��2Li��Cu2O��H2O��2Cu��2Li+��2OH-������˵���������
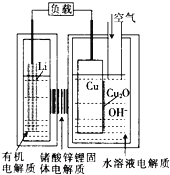
A.�ŵ�ʱ������·��ͨ��0.2mol���ӵĵ���ʱ����0.2mol Li+������������Cu���ƶ����б�״����1.12L�������뷴Ӧ
B.ͨ����ʱ��ͭ����ʴ���������Cu2O
C.�ŵ�ʱ�������ĵ缫��ӦʽΪ��Cu2O��H2O��2e-��2Cu��2OH-
D.������Ӧ���̣������е�O2���˴���������
���𰸡�D
��������
�ŵ�ʱ���ʧ������������Cu��O2�õ����������������ϵ缫��ӦʽΪLi-e-�TLi+�������ϵ缫��ӦʽΪO2+4e-+2H2O=4OH-���������Һ���������������ƶ������������ƶ����ݴ˷������
A���ŵ�ʱ����������������������ƶ������������ƶ�������·��ͨ��0.2 mol���ӵĵ���ʱ������4Cu+O2===2Cu2O��O2+4e-+2H2O=4OH-�������ϲ��뷴Ӧ������Ϊ0.05mol���ڱ�״���µ����Ϊ0.05mol��22 .4L/mol=1.12L����A��ȷ��
B���õ��ͨ��һ�ָ��ӵ�ͭ��ʴ�������������ɷ���ʽ��֪ͭ�缫�ϲ���������ֱ�ӷŵ磬������ӦΪCu2O+H2O+2e-=Cu+2OH-�����ͨ�������Ŀ������������ͭ��Ӧ����Cu2O����B��ȷ��
C���õ��ͨ��һ�ָ��ӵ�ͭ��ʴ�������������ɷ���ʽ��֪ͭ�缫�ϲ���������ֱ�ӷŵ磬������ӦΪCu2O+H2O+2e-=Cu+2OH-����C��ȷ��
D��ͨ����ʱ��ͭ����ʴ���������Cu2O���ŵ�ʱCu2Oת��ΪCu����������Ӧ�����У�ͭ�൱�ڴ�����������ΪO2����D����
�ʴ�ΪD��

����Ŀ����һ���¶��£�������X������Y ��0.16 mol����10 L �����ܱ������У�������Ӧ��X��g��+ Y��g��![]() 2Z��g�� ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±�������˵����ȷ����
2Z��g�� ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±�������˵����ȷ����
t / min | 2 | 4 | 7 | 9 |
n��Y��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.��Ӧǰ2min��ƽ������v��Z��=2.0��10-5 mol/��L��min��
B.�����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv���棩��v������
C.���¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
D.�����������䣬�ٳ���0.2 mol Z��ƽ��ʱX�����ʵ���Ũ�ȼ�С