题目内容
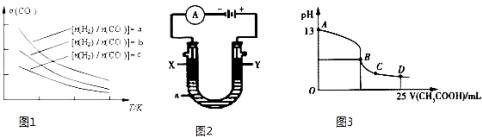
【题目】pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3。如图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5mol/L,可认为该离子不存在)。下列说法不正确的是

A.某温度下,CO2饱和溶液的浓度是0.05 molL-1,其中1/5的CO2转变为H2CO3,若此时溶液的pH约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度为0.1% ,
B.25℃时,H2CO3一级电离平衡常数的数值Ka1=10-6
C.向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣)
D.25℃时,0.1mol/LNa2CO3中c(HCO3﹣)比0.1mol/LH2CO3中c(HCO3﹣)大
【答案】C
【解析】
试题分析:A.CO2饱和溶液的浓度是0.05mol/L,其中1/5的CO2转变为H2CO3,pH=5,c(H+)=10-5mol/L,因此H2CO3的电离度为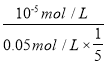 ×100%=0.1%。故A正确;B.由图象可知当pH=6时,pC(H2CO3)=pC(HCO3-),结合Ka1(H2CO3)=
×100%=0.1%。故A正确;B.由图象可知当pH=6时,pC(H2CO3)=pC(HCO3-),结合Ka1(H2CO3)=![]() =
=![]() =10-6,故B正确;C.向Na2CO3溶液中滴加盐酸至pH等于11时,根据电荷守恒,c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣)+c(Cl-),故C错误;D.根据图像,Na2CO3的一级水解常数约为10-3,H2CO3的一级电离常数约为10-4.7,因此0.1mol/LNa2CO3中c(HCO3﹣)比0.1mol/L中c(HCO3﹣)大,故D正确;故选C。
=10-6,故B正确;C.向Na2CO3溶液中滴加盐酸至pH等于11时,根据电荷守恒,c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣)+c(Cl-),故C错误;D.根据图像,Na2CO3的一级水解常数约为10-3,H2CO3的一级电离常数约为10-4.7,因此0.1mol/LNa2CO3中c(HCO3﹣)比0.1mol/L中c(HCO3﹣)大,故D正确;故选C。

 期末集结号系列答案
期末集结号系列答案【题目】短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如表:
元素编号 | 元素特征信息 |
A | 最高正价和最低负价的绝对值之差为2 |
B | 和E同主族 |
C | lmo1C单质能与冷水反应,在标准状况下生成11.2LH2 |
D | 原子最外层电子数等于其周期序数 |
E | 负一价阴离子的电子层结构与Ar原子相同 |
(1) A在周期表中的位置为 。
(2)B和C形成的化合物的电子式为 。
(3)B和D简单离子的半径大小为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是 (填序号)。
A.比较两种单质的颜色
B.比较两种单质与H2化合的难易程度
C.依据两元素在周期表中的位置
D.比较对应阴离子的还原性
e.比较最高价氧化物对应水化物的酸性
(5)E元素能与另外四种元素中的一种元素形成共价化合物,分子中的原子个数比为1∶3,相对分子质量为120.5,则该物质的化学式为 。