题目内容
5.在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3各0.01mol的混和溶液中,加入0.01mol的铁粉,经充分搅拌后,产生的变化是( )| A. | 铁溶解,析出0.01molZn | |
| B. | 铁溶解,析出铜,且溶液中不含有Fe3+ | |
| C. | 铁溶解,析出0.01molCu | |
| D. | 铁溶解,溶液中金属阳离子只剩Fe2+和Zn2+ |
分析 金属活动顺序表可知氧化性:Zn2+<Cu2+<Fe3+,充分搅拌后Fe完全反应,根据发生的反应:2Cu2++Fe═Fe2++Cu,2Fe3++Fe═3Fe2+,以此解答该题.
解答 解:在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3各0.01mol的混和溶液中,加入0.01mol的铁粉,因氧化性为Zn2+<Cu2+<Fe3+,则加入Fe粉0.01mol,发生Fe+2Fe3+=3Fe2+,铁剩余0.005mol,再发生Fe+Cu2+=Cu+Fe2+,所以Fe溶解,生成0.005molCu,溶液中阳离子为Cu2+、Zn2+、Fe2+,
故选:B.
点评 本题考查了有关氧化还原反应计算,把握反应中氧化性的强弱,明确离子氧化性顺序是解题关键,题目难度不大.

练习册系列答案
相关题目
15.3.6g某物质含有的分子数目为1.204×10 23,则该物质的摩尔质量为( )
| A. | 18 g | B. | 18 g.•mol-1 | C. | 36 g | D. | 36 g•mol-l |
20.还原性的无水草酸是无色无臭的透明结晶或白色粉末.草酸在浓硫酸并加热条件下容易脱去水分,分解为二氧化碳和一氧化碳.
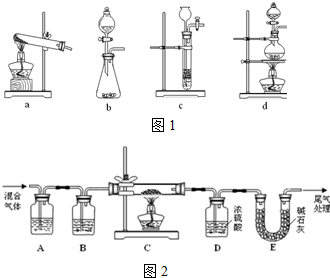
(1)草酸(H2C2O4)浓硫酸并加热条件下分解的化学方程式为:H2C2O4 $\frac{\underline{\;浓硫酸\;}}{△}$CO↑+CO2↑+H2O下列装置中如图1,可用于草酸分解制取气体的是d.(填字母)
(2)某探究小组利用草酸分解产生的混合气体和铁锈反应来测定铁锈样品组成(假定铁锈中只有Fe2O3•nH2O和Fe两种成份),实验装置如下图2所示,请回答:
①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是浓NaOH溶液、浓硫酸.
②在点燃酒精灯之前应进行的操作是:(a)检查装置气密性(或先排尽装置内空气,以防止加热时发生爆炸);(b)通入混合气体一段时间.
③准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量,硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=2(假定Fe和H2O不发生反应,实验过程中每步均完全吸收或反应).
④在本实验中,下列情况会使测定结果n偏大的是abc(填字母).
a.缺少洗气瓶B b.缺少装置E
c.反应后固体是铁和少量Fe2O3 d.反应后固体是铁和少量Fe2O3•nH2O
(3)该探究小组还利用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
①请完成以下实验设计表(表中不要留空格):
每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL,催化剂MnSO4的用量可选择0.5g、0.0g)
②若要准确计算反应速率,该实验中还需测定溶液紫色消失所需要的时间.请你设计出通过测定褪色时间长短来判断浓度大小与反应速率关系的实验方案:
取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应.
③写出KMnO4酸性溶液与H2C2O4溶液反应的离子方程式:2MnO4_+5H2C2O4+6H+=10CO2↑+8H2O+2Mn2+.

(1)草酸(H2C2O4)浓硫酸并加热条件下分解的化学方程式为:H2C2O4 $\frac{\underline{\;浓硫酸\;}}{△}$CO↑+CO2↑+H2O下列装置中如图1,可用于草酸分解制取气体的是d.(填字母)
(2)某探究小组利用草酸分解产生的混合气体和铁锈反应来测定铁锈样品组成(假定铁锈中只有Fe2O3•nH2O和Fe两种成份),实验装置如下图2所示,请回答:
①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是浓NaOH溶液、浓硫酸.
②在点燃酒精灯之前应进行的操作是:(a)检查装置气密性(或先排尽装置内空气,以防止加热时发生爆炸);(b)通入混合气体一段时间.
③准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量,硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=2(假定Fe和H2O不发生反应,实验过程中每步均完全吸收或反应).
④在本实验中,下列情况会使测定结果n偏大的是abc(填字母).
a.缺少洗气瓶B b.缺少装置E
c.反应后固体是铁和少量Fe2O3 d.反应后固体是铁和少量Fe2O3•nH2O
(3)该探究小组还利用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
①请完成以下实验设计表(表中不要留空格):
每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL,催化剂MnSO4的用量可选择0.5g、0.0g)
②若要准确计算反应速率,该实验中还需测定溶液紫色消失所需要的时间.请你设计出通过测定褪色时间长短来判断浓度大小与反应速率关系的实验方案:
| 实验 编号 | 实验目的 | T/K | 催化剂用量/g | c/mol•l-1 | |
| KMnO4 | H2C2O4 | ||||
| Ⅰ | 为以下实验作参考 | 298 | 0.5 | 0.01 | 0.1 |
| Ⅱ | 探究KMnO4酸性溶液的浓度对该反应速率的影响 | 298 | 0.5 | 0.001 | 0.1 |
| Ⅲ | 323 | 0.5 | 0.01 | 0.1 | |
| Ⅳ | 探究催化剂对反应速率的影响 | 0.1 | |||
③写出KMnO4酸性溶液与H2C2O4溶液反应的离子方程式:2MnO4_+5H2C2O4+6H+=10CO2↑+8H2O+2Mn2+.
10.下列气体中所含原子数最多的是( )
| A. | 标准状况下44.8L H2 | B. | 88gCO2 | ||
| C. | 9.03ⅹ1023个CH4 分子 | D. | 3molH2O |
17.100mL6mol/L的硫酸跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
①硫酸钠固体 ②水 ③硫酸钾溶液 ④硝酸钾溶液 ⑤CuSO4溶液.
①硫酸钠固体 ②水 ③硫酸钾溶液 ④硝酸钾溶液 ⑤CuSO4溶液.
| A. | ①②⑤ | B. | ①④ | C. | ②③ | D. | ③④⑤ |
15.下列说法中错误的是?( )
| A. | 有机物和无机物都可以从动植物的有机体中获取? | |
| B. | 所有有机物在一定条件下都能相互转化? | |
| C. | 有机物和无机物在性质上的差别不是绝对的 | |
| D. | 有机物参与的反应,一般比较复杂,速率较慢,且常伴有副反应发生? |
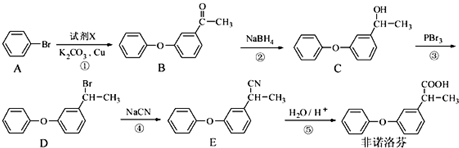
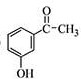 .
.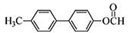 .
.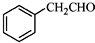 为原料制备
为原料制备 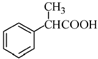 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH$→_{浓硫酸△}^{CH_{3}COOH}$CH3COOCH2CH3合成路线流程图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH$→_{浓硫酸△}^{CH_{3}COOH}$CH3COOCH2CH3合成路线流程图: .
.