题目内容
16.下列所含分子数由多到少的排列顺序是C>B>A>DA.标准状况下33.6LH2
B.所含电子的物质的量为4mol的H2
C.20℃时45g H2O
D.常温下,16g O2与14g N2的混合气体.
分析 A.根据n=$\frac{V}{{V}_{m}}$计算氢气的物质的量;
B.结合氢气分子含有电子数目计算氢气的物质的量;
C.根据n=$\frac{m}{M}$计算水的物质的量;
D.根据n=$\frac{m}{M}$计算氧气、氮气的物质的量,进而计算总的物质的量.
解答 解:A.标准状况下33.6LH2的物质的量为$\frac{33.6L}{22.4L/mol}$=1.5mol;
B.每个氢气分子含有2个电子,故含有电子的物质的量为4mol的H2的物质的量为$\frac{4mol}{2}$=2mol;
C.20℃,45gH2O的物质的量为$\frac{45g}{18g/mol}$=2.5mol;
D.16gO2的物质的量为$\frac{16g}{32g/mol}$=0.5mol,14gN2的物质的量为$\frac{14g}{28g/mol}$=0.5mol,混合气体总的物质的量为1mol;
根据N=nNA可知,物质的量越大含有分子数目越多,故分子数目由多到少的顺序为C>B>A>D;
故答案为:C>B>A>D.
点评 本题考查常用化学计量的有关计算,比较基础,注意对公式的理解与灵活运用,注意理解分子中微粒数目的计算.

练习册系列答案
相关题目
4.下列实验操作中错误的是( )
| A. | 蒸发操作时,当溶液中出现较多固体应停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 如果没有试管夹,可以临时手持试管给固体或液体加热 |
1.下列物质所属的类别及其所含官能团的对应关系不正确的是( )
| A. | CH3CH=CH2 烯烃 | B. |  羧酸-COOH 羧酸-COOH | ||
| C. |  醛类 醛类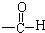 | D. | RCH2OH (R为烃基) 醇类-OH |
8.下列叙述正确的是( )
| A. | 摩尔质量就等于该物质的相对分子质量或相对原子质量 | |
| B. | 硫酸的摩尔质量是98克 | |
| C. | 1molH2O的质量为18克 | |
| D. | 2molH2O的质量为18克 |
5.在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3各0.01mol的混和溶液中,加入0.01mol的铁粉,经充分搅拌后,产生的变化是( )
| A. | 铁溶解,析出0.01molZn | |
| B. | 铁溶解,析出铜,且溶液中不含有Fe3+ | |
| C. | 铁溶解,析出0.01molCu | |
| D. | 铁溶解,溶液中金属阳离子只剩Fe2+和Zn2+ |
6.利用下述方法除去氮气中所含的杂质(HCl,H2,H2S)以得到干燥纯净氮气,在下列各步中应采用的正确顺序是( )
①通过装有变色硅胶的干燥管 ②通过氢氧化钠溶液 ③通过加热的氧化铜.
①通过装有变色硅胶的干燥管 ②通过氢氧化钠溶液 ③通过加热的氧化铜.
| A. | ①②③③ | B. | ②①③① | C. | ②③③① | D. | ③②①③ |
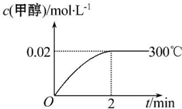 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应为CO(g)+2H2(g)═CH3OH(g)△H<0.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应为CO(g)+2H2(g)═CH3OH(g)△H<0.