题目内容
15.3.6g某物质含有的分子数目为1.204×10 23,则该物质的摩尔质量为( )| A. | 18 g | B. | 18 g.•mol-1 | C. | 36 g | D. | 36 g•mol-l |
分析 根据n=$\frac{N}{{N}_{A}}$计算该物质的物质的量,再根据M=$\frac{m}{n}$计算其相对分子质量,进而确定可能的组成.
解答 解:3.6g某物质中含有1.204×1023个分子,其物质的量为$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}}$=0.2mol,其相对分子质量为$\frac{3.6}{0.2}$=18,则摩尔质量为18g/mol,故选B.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
3.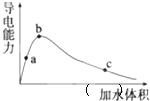 25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法正确的是( )
25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法正确的是( )
 25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法正确的是( )
25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法正确的是( )| A. | 醋酸的电离平衡常数:a<b<c | |
| B. | 溶液中n(H+):b>a>c | |
| C. | a、b、c三点的溶液都有:c(H+)=c(CH3COO-)+c(OH-) | |
| D. | 从c点到b点,醋酸的电离度不断增大 |
20.某实验小组设计实验测定Na2S04和Na2C03混合物中各组分的含量.
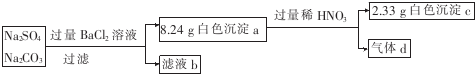
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 沉淀a的主要成分是BaS04和BaC03 | |
| B. | 滤液b中Na+的物质的量为0.08 mol | |
| C. | 气体d在标准状况下的体积为224 mL | |
| D. | 原混合物中Na2S04与Na2C03的物质的量之比为1:3 |
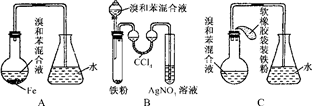
4.下列实验操作中错误的是( )
| A. | 蒸发操作时,当溶液中出现较多固体应停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 如果没有试管夹,可以临时手持试管给固体或液体加热 |
5.在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3各0.01mol的混和溶液中,加入0.01mol的铁粉,经充分搅拌后,产生的变化是( )
| A. | 铁溶解,析出0.01molZn | |
| B. | 铁溶解,析出铜,且溶液中不含有Fe3+ | |
| C. | 铁溶解,析出0.01molCu | |
| D. | 铁溶解,溶液中金属阳离子只剩Fe2+和Zn2+ |
 .
. 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题:
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题: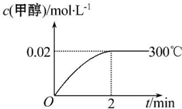 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应为CO(g)+2H2(g)═CH3OH(g)△H<0.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应为CO(g)+2H2(g)═CH3OH(g)△H<0.