题目内容
13.氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品.某研究小组用粗铜(含杂质Fe)按如图1流程制备氯化铜晶体(CuCl2•2H2O),已知氯化铜易溶于水,难溶于乙醇.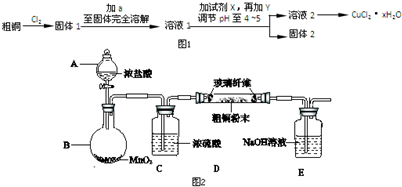
(1)溶液1中的金属离子有Fe3+、Fe2+、Cu2+.能检验溶液1中Fe2+的试剂①②(填编号)
①KMnO4②K3[Fe(CN)6]③NaOH④KSCN
为了更完全的沉淀,试剂X为H2O2.
(2)试剂a是盐酸,加入需过量的原因是充分反应,抑制Cu2+水解.试剂Y用于调节pH以除去杂质,Y可选用下列试剂中的cd(填序号).
a.NaOH b.NH3•H2O c.CuO d.Cu2(OH)2CO3 e.CuSO4
调节pH至4~5的原因是使溶液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀.
得到固体2的操作是过滤.
(3)实验室采用如图2所示的装置,可将粗铜与Cl2反应转化为固体1(部分加热和夹持装置已略去).
①仪器A的名称是分液漏斗.
②引发B中反应的操作是打开分液漏斗上口玻璃塞,旋开分液漏斗活塞,缓慢滴加,并用酒精灯加热B装置.
装置B中发生反应的离子方程式是+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要否(填“是”或“否”).
理由是HCl对反应没有影响,且可以抑制氯化铜水解.
(4)实验所需480mL10mol/L浓HCl配制时用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、500mL容量瓶.
(5)实验结束时,B和D处酒精灯应先熄灭的是D.
(6)在溶液2转化为CuCl2•xH2O的操作过程中,发现溶液颜色由蓝色变为绿色.小组同学欲探究其原因.
已知:在氯化铜溶液中有如下转化关系:Cu(H2O)42+(aq)+4Cl-(aq)?CuCl42-(aq)+4H2O(l)
蓝色 黄色
①上述反应的化学平衡常数表达式是K=$\frac{c(CuC{{l}_{4}}^{2-})}{c[Cu({H}_{2}O{)_{4}}^{2+}]•{c}^{4}(C{l}^{-})}$.若增大氯离子浓度,K值不变(填“增大”、“减小”或“不变”).
②取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是abc(填序号).
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
(7)该装置存在缺陷,请写出:缺少防止倒吸装置安全瓶.请画出增加后的装置.
(8)得到CuCl2•xH2O晶体最好采用的干燥方式是D.
A.空气中加热蒸干 B.空气中低温蒸干 C.HCl气流中加热烘干 D.HCl气流中低温烘干
(9)为了测定制得的氯化铜晶体(CuCl2•xH2O)中x的值,某兴趣小组设计了以下实验方案:
称取m g晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再轻为止,冷却,称量所得黑色固体的质量为ng.沉淀洗涤的操作方法是向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次,根据实验数据测得x=$\frac{80m-135n}{18n}$(用含m、n的代数式表示).
分析 粗铜中含有Fe,与氯气反应生成CuCl2和FeCl3,为防止水解,应加入过量的稀盐酸进行溶解,并保证金属完全反应,溶液1中的金属离子有Fe3+、Fe2+、Cu2+,加入试剂X目的是将溶液中Fe2+氧化为Fe3+,应为H2O2,还原得到水,是绿色氧化剂,通过调节pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤分离,且加入Y可以消耗氢离子且不能引入新杂质,可以为CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3.滤液经过加热浓缩、冷却结晶、过滤、洗涤、干燥得到CuCl2•2H2O.
(1)Fe2+具有还原性,可以使酸性高锰酸钾溶液褪色;能与K3[Fe(CN)6]反应得到蓝色铁氰化亚铁蓝色沉淀;
加入试剂X目的是将溶液中Fe2+氧化为Fe3+,最好应为H2O2;
(2)调节pH至4~5之间,液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀,过滤分离;得到固体2的操作是将不溶固体与液体进行分离;
(3)B装置中二氧化锰与浓盐酸在加热条件下反应生成氯气,C装置干燥氯气,D装置中粗铜(Fe、Cu的混合物)与氯气反应生成CuCl2和FeCl3,多于的氯气用氢氧化钠溶液吸收,以防污染空气,由于HCl不影响氯气和粗铜的反应的产物,且可以抑制氯化铜水解,氯气中混有的HCl不需要除去;
(4)实验所需480mL10mol/L浓HCl配制时用到的玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管、500mL容量瓶;
(5)防止E中溶液倒吸,发生危险;
(6)①平衡常数为生成物浓度化学计量数次数幂乘积与反应物浓度化学计量数次数幂乘积的比值;
平衡常数只受温度影响,与离子浓度无关;
②稀溶液中以Cu(H2O)42+为主,呈蓝色,浓溶液中以CuCl42-为主,呈黄色,一定浓度下呈蓝绿色,结合平衡移动原理分析;
(7)该装置缺少防止倒吸装置,在D、E之间添加防倒吸的安全瓶;
(8)CuCl2•xH2O晶体加热容易分解,且氯化铜易水解,应在HCl气流中低温烘干
(9)氯化铜溶液中加入足量氢氧化钠溶液、过滤得到沉淀为氢氧化铜,沉淀洗涤的操作方法是:向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次;
氢氧化铜加热分解所得黑色固体的质量ng为CuO,根据Cu元素守恒计算CuCl2•xH2O的物质的量,再结合m=nM计算x的值.
解答 解:粗铜中含有Fe,与氯气反应生成CuCl2和FeCl3,为防止水解,应加入过量的稀盐酸进行溶解,并保证金属完全反应,溶液1中的金属离子有Fe3+、Fe2+、Cu2+,加入试剂X目的是将溶液中Fe2+氧化为Fe3+,应为H2O2,还原得到水,是绿色氧化剂,通过调节pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤分离,且加入Y可以消耗氢离子且不能引入新杂质,可以为CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3.滤液经过加热浓缩、冷却结晶、过滤、洗涤、干燥得到CuCl2•2H2O.
(1)①Fe2+具有还原性,可以使酸性高锰酸钾溶液褪色,用高锰酸钾溶液可以检验Fe2+,故正确;
②Fe2+能与K3[Fe(CN)6]反应得到蓝色铁氰化亚铁蓝色沉淀,故正确;
③铁离子、铜离子均与NaOH反应生成沉淀,影响亚铁离子检验,故错误;
④铁离子与KSCN反应,溶液呈红色,不能检验Fe2+,故错误;
加入试剂X目的是将溶液中Fe2+氧化为Fe3+,X应为H2O2,还原得到水,是绿色氧化剂,
故答案为:①②;H2O2;
(2)由上述分析可知,试剂X为盐酸,加入过量的盐酸,充分反应,抑制Cu2+水解;
加入Y可以消耗氢离子调节溶液pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤分离,且不能引入新杂质,
a.NaOH引入杂质钠离子,故a错误;
b.NH3•H2O 引入铵根离子,故b错误;
c.CuO可以调节PH值,除去杂质,过量的CuO过滤除去,不引入杂质,故c正确;
d.Cu2(OH)2CO3 可以调节PH值,除去杂质,过量的Cu2(OH)2CO3 过滤除去,不引入杂质,故d正确;
e.CuSO4不能调节PH值,引入硫酸根离子,故e错误;
调节pH至4~5之间,使溶液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀;
得到固体2的操作是将不溶固体与液体进行分离,应采取过滤操作,
故答案为:盐酸;充分反应,抑制Cu2+水解;cd;使溶液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀;过滤;
(3)B装置中二氧化锰与浓盐酸在加热条件下反应生成氯气,C装置干燥氯气,D装置中粗铜(Fe、Cu的混合物)与氯气反应生成CuCl2和FeCl3,多于的氯气用氢氧化钠溶液吸收,以防污染空气,由于HCl不影响氯气和粗铜的反应的产物,且可以抑制氯化铜水解,氯气中混有的HCl不需要除去.
①仪器A是分液漏斗,故答案为:分液漏斗;
②引发B中反应的操作是:打开分液漏斗上口玻璃塞,旋开分液漏斗活塞,缓慢滴加,并用酒精灯加热B装置;装置B中制取氯气,二氧化锰与浓盐酸发生反应生成氯化锰、氯气、水,反应离子方程式为:+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
故答案为:打开分液漏斗上口玻璃塞,旋开分液漏斗活塞,缓慢滴加,并用酒精灯加热B装置;MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
③HCl对反应没有影响,且可以抑制氯化铜水解,不需要在浓硫酸洗气瓶前增加吸收HCl的装置,
故答案为:否;HCl对反应没有影响,且可以抑制氯化铜水解;
(4)实验所需480mL10mol/L浓HCl配制时用到的玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管、500mL容量瓶,
故答案为:量筒、烧杯、玻璃棒、胶头滴管、500mL容量瓶;
(5)应向熄灭D处酒精灯,后熄灭B处酒精灯,防止E中溶液倒吸,发生危险,故答案为:D;
(6)①Cu(H2O)42+(aq)+4Cl-(aq)?CuCl42-(aq)+4H2O(l)的平衡常数为K=$\frac{c(CuC{{l}_{4}}^{2-})}{c[Cu({H}_{2}O{)_{4}}^{2+}]•{c}^{4}(C{l}^{-})}$,
平衡常数只受温度影响,与离子浓度无关,增大氯离子浓度,K值不变,
故答案为:$\frac{c(CuC{{l}_{4}}^{2-})}{c[Cu({H}_{2}O{)_{4}}^{2+}]•{c}^{4}(C{l}^{-})}$;不变;
②a.将Y稀释,平衡向左反应移动,溶液呈蓝色,可以能够证明CuCl2溶液中转化关系,故a正确;
b.在Y中加入CuCl2晶体,溶液中Cu(H2O)42+浓度增大,平衡向右移动,溶液变为绿色,可以能够证明CuCl2溶液中转化关系,故b正确;
c.在Y中加入NaCl固体,溶液中氯离子浓度增大,平衡向右移动,溶液变为绿色,可以能够证明CuCl2溶液中转化关系,故c正确;
d.取Y进行电解,铜离子放电,溶液颜色最终消失,不能可以能够证明CuCl2溶液中转化关系,故d错误.
故选:abc;
(7)该装置缺少防止倒吸装置,在D、E之间添加防倒吸的安全瓶,如图所示:
故答案为:缺少防止倒吸装置安全瓶; ;
;
(8)CuCl2•xH2O晶体加热容易分解,且氯化铜易水解,应在HCl气流中低温烘干,故答案为:D;
(9)氯化铜溶液中加入足量氢氧化钠溶液、过滤得到沉淀为氢氧化铜,沉淀洗涤的操作方法是:向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次;
氢氧化铜加热分解所得黑色固体的质量ng为CuO,根据Cu元素守恒:n(CuCl2•xH2O)=n(CuO)=$\frac{n}{80}$mol,则$\frac{n}{80}$mol×(135+18x)=mg,解得x=$\frac{80m-135n}{18n}$,
故答案为:向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次;$\frac{80m-135n}{18n}$.
点评 本题考查化学工艺流程及实验制备,涉及对实验装置与操作及试剂的分析评价、物质分离提纯、化学平衡移动、化学计算等,要求学生具备扎实的基础与综合运用能力,难度很大.

 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案| A. | 向NaHCO3溶液中加入足量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- | |
| B. | 向亚硫酸钠溶液中滴入少量新制的氯水:3SO32-+Cl2+H2O=SO42-+2Cl-+2HSO3- | |
| C. | 电解KBr溶液时阴极的电极反应式为:K++e-=K | |
| D. | 将Fe2O3固体投入到少量HI溶液中:Fe2O3+6H++6I-=2Fe2++3I2+3H2O |
| A. | 氧气和臭氧(O3)是氧元素的同素异形体 | |
| B. | 乙酸和甲酸甲酯是同分异构体 | |
| C. | 12C和13C互为同位素 | |
| D. | 软脂酸(C15H31COOH)和油酸(C17H33COOH)是同系物 |
| A. | $\frac{3}{8}$ mol | B. | $\frac{8}{3}$ mol | C. | $\frac{2}{3}$ mol | D. | $\frac{3}{2}$ mol |
| A. | 对废旧电池进行回收处理 | |
| B. | 禁止生产、销售、使用超薄塑料购物袋 | |
| C. | 对聚乙烯等塑料垃圾进行深埋或倾倒入海 | |
| D. | 使用沼气、太阳能、风能等能源替代传统的煤炭 |
| A | ||
| B | C | D |
(2)元素A在化合物中一般显负(填正或负)价,但在与F(填元素符号)形成化合物时,所显示的价态正好相反.
(3)比较C、D元素简单离子半径的大小S2->Cl-(填离子符号).
(4)向D与E形成的化合物的水溶液中加入过量氨水,有关反应的离子方程式为Mg2++2 NH3.H2O═Mg (OH)2↓+2 NH4+.
(5)D的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的化学方程式为Mg(OH)2+2HClO4═Mg(ClO4)2+2H2O.
| A. | 用重结晶的方法分离苯甲酸和氯化钠的混合物 | |
| B. | 用苯和溴水在Fe催化下可制得溴苯 | |
| C. | 用乙醇、冰醋酸和pH=1的H2SO4溶液混合加热可制备乙酸乙酯 | |
| D. | 将电石与水反应后的气体直接通入到溴水中,可以验证乙炔能使溴水褪色的性质 |
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
| A. | K+、Cl-、SO${\;}_{4}^{2-}$、Al3+ | B. | Fe2+、NO${\;}_{3}^{-}$、Na+、Cl- | ||
| C. | S2-、Na+、NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$ | D. | SO${\;}_{3}^{2-}$、K+、NO${\;}_{3}^{-}$、Cl- |