题目内容
3.下列在酸性溶液中能大量共存的离子组是( )| A. | K+、Cl-、SO${\;}_{4}^{2-}$、Al3+ | B. | Fe2+、NO${\;}_{3}^{-}$、Na+、Cl- | ||
| C. | S2-、Na+、NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$ | D. | SO${\;}_{3}^{2-}$、K+、NO${\;}_{3}^{-}$、Cl- |
分析 A.四种离子之间不反应,都不与酸性溶液中的氢离子反应;
B.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子;
C.硝酸根离子在酸性条件下能够氧化硫离子;
D.硝酸根离子在酸性溶液中能够氧化亚硫酸根离子.
解答 解:A.K+、Cl-、SO42-、Al3+之间不反应,都不与酸性溶液中的氢离子反应,在溶液中能够大量共存,故A正确;
B.NO3-在酸性溶液中具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故B错误;
C.NO3-在酸性溶液中具有强氧化性,能够氧化S2-,在溶液中不能大量共存,故C错误;
D.NO3-在酸性溶液中具有强氧化性,能够氧化SO32-,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存,题目难度中等,明确离子反应发生条件为解答关键,注意掌握离子共存的条件,本题中特别注意硝酸根离子在酸性条件下具有强氧化性,能够氧化具有还原性的离子,如:Fe2+、SO32-、S2-,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
11.下列说法不正确的是( )
| A. | 某微粒空间构型为三角锥形,则该微粒一定是极性分子 | |
| B. | 某微粒空间构型为V形,则中心原子一定有孤电子对 | |
| C. | NH4+中N-H键能、键长和键角均相同 | |
| D. | SiF4和SO${\;}_{3}^{2-}$的中心原子均为sp3杂化,其立体构型都是正四面体 |
8.依据元素周期律,下列推断中正确的是( )
| A. | KOH比NaOH碱性强 | |
| B. | H3BO3的酸性比H2CO3的酸性强 | |
| C. | HCl、H2S、H3P的还原性性逐渐减弱 | |
| D. | 若M+和R2-的核外电子层结构相同,则离子半径M+>R2- |
15.在以下的分子或离子中,空间结构的几何形状不是三角锥形的是( )
| A. | NF3 | B. | CH${\;}_{3}^{-}$ | C. | SO3 | D. | H3O+ |
12.下列有关电解质溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 在0.1mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) | |
| B. | 在0.1mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
13.有A、B、C、D四种金属,分别把它们加入到稀盐酸中,A、B、D反应后有气体放出,C无明显现象,再把A、D加入B盐溶液中,D表面有B析出,而A没有,则四种金属的活动性顺序是为( )
| A. | A>B>D>C | B. | B>D>A>C | C. | D>A>B>C | D. | D>B>A>C |
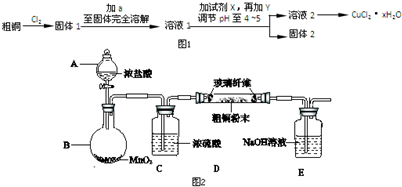
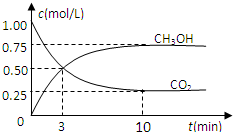 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.