题目内容
1.经测定C3H7OH和C6H12组成的混合物中氢的质量分数为14%,则此混合物中碳的质量分数为78%.分析 C3H7OH可以将写成C3H6•H2O,C3H6和C6H12中C、H原子数目之比为1:2,原混合物可以看做CH2、H2O的混合物,设混合物中CH2的质量分数为x,则H2O的质量分数为(1-x),表示出CH2、H2O中氢元素的质量分数,利用氢元素质量分数列方程计算,再根据化学式CH2计算碳元素质量分数.
解答 解:C3H7OH可以将写成C3H6•H2O,C3H6和C6H12中C、H原子数目之比为1:2,原混合物可以看做CH2、H2O的混合物,
设混合物中CH2的质量分数为x,则H2O的质量分数为(1-x),
则CH2中H元素质量分数为$\frac{1}{7}$x,则H2O中H元素质量分数为$\frac{1}{9}$(1-x),
故$\frac{1}{7}$x+$\frac{1}{9}$(1-x)=14%,解得x=91%,
故混合物中碳元素质量分数为91%×$\frac{6}{7}$=78%,
故答案为:78%.
点评 本题考查混合物计算,涉及质量分数计算,注意利用改写法简化计算过程,侧重考查学生分析计算能力.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
9.已知:某温度时,KW=1.0×10-12.在该温度下,测得0.1mol•L-1Na2A溶液pH=6,则下列说法正确的是( )
| A. | H2A在水溶液中的电离方程式为:H2A=H++HA-,HA-?H++A2- | |
| B. | 常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(A2-) | |
| C. | 相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等 | |
| D. | 0.0l mol•L-l的NaHA溶液pH>2 |
16.下列有关粒子组的评价及相关离子方程式均正确的是( )
| 选项 | 粒子组 | 评价及离子方程式 |
| A | K+、Al3+、SO42-、NO3- | 能大量共存于同一溶液中 |
| B | H+、CH3CHO、SO42-、MnO4- | 能大量共存于同一溶液中 |
| C | NH4+、Fe3+、SCN-、Cl- | 不能大量共存,Fe3++3SCN-=Fe(SCN)3↓ |
| D | Na+、K+、HCO3-、OH- | 不能大量共存,HCO3-+OH-=H2O+CO2↑ |
| A. | A | B. | B | C. | C | D. | D |
6.下列各晶体中任意一个原子都被相邻的4个原子所包围:以共价键结合成正四面体结构,并向空间伸展成网状结构的是( )
| A. | 甲烷 | B. | 石墨 | C. | 晶体硅 | D. | 水晶 |
13.化学与社会、生活密切相关,下列说法正确的是( )
| A. | 加碘食盐中添加的是碘化钾 | |
| B. | 味觉上具有酸味的食物就是酸性食物 | |
| C. | Fe3O4俗称铁红,常做红色油漆和涂料 | |
| D. | 晶体硅具有半导体性质,可用于生产计算机芯片 |
12.下列关于材料的说法中,正确的是( )
| A. | 硅的提纯与应用,促进了半导体元件与集成芯片的发展 | |
| B. | 水泥、玻璃、塑料都是高分子材料 | |
| C. | 钢化玻璃与普通玻璃的主要成分不同 | |
| D. | 通常情况下,铝合金在空气中不易被腐蚀,可用做建筑材料 |
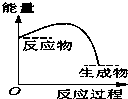
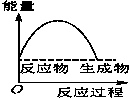
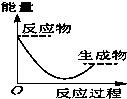
 将某固体氢氧化物M与NH4Cl置于如图所示的装置(玻璃片与烧杯底部之间有一薄层水)中混合反应后,用手拿起烧杯时,发现玻璃片与烧杯粘在一起,则该反应所对应的能量变化关系图是( )
将某固体氢氧化物M与NH4Cl置于如图所示的装置(玻璃片与烧杯底部之间有一薄层水)中混合反应后,用手拿起烧杯时,发现玻璃片与烧杯粘在一起,则该反应所对应的能量变化关系图是( )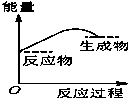

 SO42-+CaCO3.
SO42-+CaCO3.