题目内容
16.下列有关粒子组的评价及相关离子方程式均正确的是( )| 选项 | 粒子组 | 评价及离子方程式 |
| A | K+、Al3+、SO42-、NO3- | 能大量共存于同一溶液中 |
| B | H+、CH3CHO、SO42-、MnO4- | 能大量共存于同一溶液中 |
| C | NH4+、Fe3+、SCN-、Cl- | 不能大量共存,Fe3++3SCN-=Fe(SCN)3↓ |
| D | Na+、K+、HCO3-、OH- | 不能大量共存,HCO3-+OH-=H2O+CO2↑ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.四种离子之间不发生反应,能够大量共存;
B.酸性条件下高锰酸根离子能够氧化乙醛;
C.铁离子与硫氰根离子反应生成络合物硫氰化铁,不是沉淀;
D.碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水,不会生成二氧化碳气体.
解答 解:A.K+、Al3+、SO42-、NO3-之间不发生反应,在溶液中能够大量共存,该选项中的评价及离子方程式都合理,故A正确;
B.MnO4-和CH3CHO发生氧化还原反应,在溶液中不能大量共存,该评价不合理,故B错误;
C.离子方程式书写错误,Fe(SCN)3不是沉淀,不应该有沉淀符号,正确的离子方程式为:Fe3++3SCN-=Fe(SCN)3,故C错误;
D.HCO3-、OH-之间反应生成碳酸根离子和水,不会生成二氧化碳,正确的离子方程式为:HCO3-+OH-=H2O+CO32-,故D错误;
故选A.
点评 本题考查离子共存、离子方程式的判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确判断离子能否共存的常用方法,本题需要注意从“评价、相关离子方程式”两个方面分析,为易错点.

练习册系列答案
相关题目
7.下列指定反应的离子方程式正确的是( )
| A. | Cu与浓硝酸反应制备NO2:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O | |
| B. | NH4Al(SO4)2溶液与过量NaOH溶液反应:Al3++4OH-═AlO2-+2H2O | |
| C. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| D. | 用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2═I2+2OH- |
4.某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等.为确定该溶液X的成分,某学习小组做了如下实验:

则下列说法正确的是( )

则下列说法正确的是( )
| A. | 若含有Fe3+,则一定含有Cl- | |
| B. | SO42-、NH4+一定存在,NO3-、Cl-可能不存在 | |
| C. | CO32-、Al3+、K+一定不存在 | |
| D. | 气体甲、沉淀甲一定为纯净物 |
11.能正确表示下列反应的离子方程式是( )
| A. | Ba(OH)2溶液中加入少量的NaHSO4溶液中:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | SO2通入NaCO溶液中:SO2+ClO-+2OH-=SO42-+Cl-+H2O | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ | |
| D. | 用H2O2从酸化的海带灰浸出液中提取I2:H2O2+2I-=I2+2OH- |
8.下列表示对于化学反应的离子方程式正确的是( )
| A. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 误将洁厕灵与84消毒液混合:H++Cl-+HClO=Cl2↑+H2O | |
| C. | 酸性高锰酸钾和过氧化氢制取少量氧气:2MnO4-+12H++4H2O2═4Mn2++7O2↑+10H2O | |
| D. | 用0.3mol/L的氯化铵溶液除去氢氧化铝中少量的氢氧化镁:Mg(OH)2+2NH4+=Mg2++2NH3•H2O |
5.下列有关实验原理或操作正确的是( )
| A. | 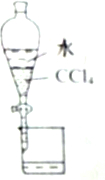 分离CCl4和水 | |
| B. |  洗涤沉淀时,向漏斗中加适量水,搅拌并滤干 | |
| C. |  液体分层,下层呈无色 | |
| D. |  除去氯气中的氯化氢 |
7.有机物CH3-CH=CH-Cl能发生的反应有( )
①取代反应 ②加成反应 ③消去反应 ④使溴的四氯化碳溶液褪色
⑤聚合反应 ⑥使酸性高锰酸钾溶液褪色.
①取代反应 ②加成反应 ③消去反应 ④使溴的四氯化碳溶液褪色
⑤聚合反应 ⑥使酸性高锰酸钾溶液褪色.
| A. | 全部 | B. | 除⑤外 | C. | 除①外 | D. | 除①、⑤外 |