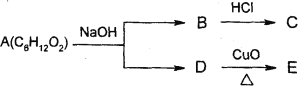
题目内容
【题目】常见的太阳能电池有单晶硅或多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。请回答下列问题:
(1)基态硒原子的价电子排布式为___;H2O的沸点高于H2Se的沸点(-42℃),其原因是___。
(2)已知GaCl3晶体熔点为77.9℃,沸点为201.3℃,GaCl3品体类型为____。
(3)Na3AsO4中阴离子的空间构型为_____,As原子采取_____杂化。
(4)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因:_____。
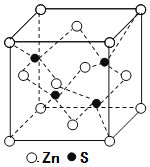
(5)锌与铜位于同一周期。硫化锌的晶胞结构如图所示,S2-周围等距离且最近的Zn2+个数为____;若晶胞边长为dpm,则硫化锌的密度为____g·cm-3(不必简化)。
【答案】4s24p4 水分子之间存在氢键,H2Se分子之间不存在氢键 分子晶体 正四面体 sp3 Cu2O中Cu+价层电子排布处于稳定的全充满状态 4 ![]()
【解析】
(1)硒为34号元素,有6个价电子,所以硒的价层电子排布式为4s24p4;水分子之间存在氢键,H2Se分子之间不存在氢键,所以沸点高低:H2O>H2Se,故答案为:4s24p4;水分子之间存在氢键,H2Se分子之间不存在氢键;
(2)根据题中信息,GaCl3的熔点较低,GaCl3为分子晶体,故答案为:分子晶体;
(3)Na3AsO4中阴离子AsO43—,AsO43—中As原子价层电子对数为4,孤对电子数为0,所以As原子采取sp3杂化,AsO43—的空间构型为正四面体,故答案为:正四面体;sp3;
(4)原子轨道处于全空、半满或全满时最稳定,CuO中Cu2+的价层电子排布为3d9结构,而Cu2O中Cu+价层电子排布为全充满的3d10结构,更稳定,所以高温下CuO容易转化为Cu2O,故答案为:Cu2O中Cu+价层电子排布处于稳定的全充满状态;
(5)根据硫化锌晶胞结构图可知,每个Zn2+周围有4个S2-,每个S2-周围也有4个Zn2+;该晶胞中含有Zn2+数为8×![]() +6×
+6×![]() =4,含S2-数为4,则依据质量关系可得
=4,含S2-数为4,则依据质量关系可得![]() =(d×10-10cm)3ρ,则硫化锌的密度ρ=
=(d×10-10cm)3ρ,则硫化锌的密度ρ=![]() g·cm-3,故答案为:4;
g·cm-3,故答案为:4;![]() 。
。

 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】I.已知,常温下H2S、H2CO3的电离常数如表
Ka1 | Ka2 | |
H2S | 9.1×10-8 | 1×10-15 |
H2CO3 | 4.3×10-7 | 5.6×10-11 |
(1)①常温下,0.1 mol·L-1的硫化钠溶液和0.1mol·L-1的碳酸钠溶液,碱性更强的是_______。其原因是_____________________________。
②常温下,硫化钠水解的离子方程式为_____________________________。
(2)常温下,向100mL0.1mol·L-1H2S溶液中滴加0.1mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
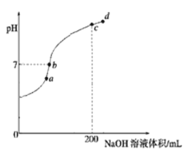
试分析图中a、b、c、d四个点,水的电离程度最大的是________。
II.减少NO2、SO2、CO等有害气体对大气环境的危害,是人类的共同追求。
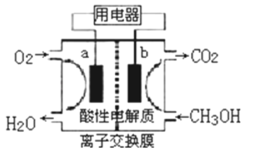
(3)以甲醇做燃料的电池,如图所示,其负极反应式为________,该燃料电池在理想状态下,将有96.5%的化学能转化成电能,即消耗1mol液体甲醇所能产生的最大电能达702.1kJ,则通常甲醇燃烧的热化学反应方程式为________。
(4)已知:NO2(g)+SO2(g)![]() SO3(g)+NO(g) △H=+41.8kJmol﹣1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的________。
SO3(g)+NO(g) △H=+41.8kJmol﹣1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1molSO3的同时生成1molNO2
(5)当上述反应平衡时,测得NO2与SO2体积比为1:6,则平衡常数K=________。