题目内容
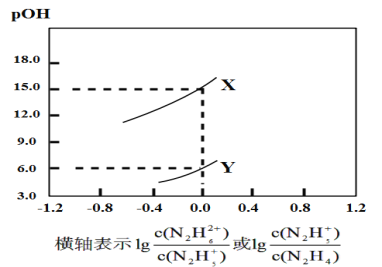
【题目】![]() 时,下列各溶液中有关微粒的物质的量浓度关系正确的是
时,下列各溶液中有关微粒的物质的量浓度关系正确的是![]()
![]()
A.向![]() 溶液中滴加NaOH溶液至恰好呈中性:
溶液中滴加NaOH溶液至恰好呈中性:![]()
B.![]() 溶液呈酸性:
溶液呈酸性:![]()
C.![]() 溶液与
溶液与![]() 溶液混合后的酸性溶液:
溶液混合后的酸性溶液:![]() COO
COO![]()
D.浓度均为![]() 的小苏打溶液与烧碱溶液等体积混合:
的小苏打溶液与烧碱溶液等体积混合:![]()
【答案】D
【解析】
A.根据物料守恒可得:![]() ,则
,则![]() ;由于溶液为中性,则
;由于溶液为中性,则![]() ,根据电荷守恒可得:
,根据电荷守恒可得:![]()
![]() ,所以
,所以![]()
![]() ,结合
,结合![]() 可知:
可知:![]()
![]() ,所以溶液中离子浓度大小为:
,所以溶液中离子浓度大小为:![]() ,故A错误;
,故A错误;
B.![]() 溶液呈酸性,说明
溶液呈酸性,说明![]() 电离程度大于水解程度,所以
电离程度大于水解程度,所以![]() ,但是其电离和水解程度都较小,则存在
,但是其电离和水解程度都较小,则存在![]() ,故B错误;
,故B错误;
C.二者混合后,溶液中溶质为等物质的量浓度的 ![]() 、NaCl、
、NaCl、![]() ,溶液中存在电荷守恒
,溶液中存在电荷守恒![]() 、存在物料守恒
、存在物料守恒![]() ,所以存在
,所以存在![]() ,故C错误;
,故C错误;
D.等浓度、等体积的小苏打和烧碱溶液混合,二者恰好完全反应生成![]() ,溶液中存在电荷守恒得
,溶液中存在电荷守恒得![]() ,故D正确。
,故D正确。
故选D。

【题目】如图是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)写出⑧的氢化物和②的氢化物反应的化学方程式________。
(2)在元素①~⑧中,非金属性最强的元素是________(填元素名称)。
(3)写出元素②的最高价氧化物对应水化物的电离方程式________。
(4)写出⑤⑧最高价氧化物的水化物之间的离子反应________________。
(5)由②和⑧组成的化合物中各原子均满足稳定结构,写出该化合物的结构式________________。
【题目】溶液X中含有右表离子中的某5种,且其浓度均为![]() 不考虑水的电离与离子水解
不考虑水的电离与离子水解![]() 向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
阳离子 | 阴离子 |
Fe Fe |
|
A.X溶液中不可能含有![]() 或
或![]()
B.生成无色气体的离子方程式为:![]()
C.根据电荷守恒,原溶液中一定含![]()
D.X溶液中一定含3种阳离子、2种阴离子