题目内容
16.苯是重要的化工原料,如图是某酮酸E的合成路线.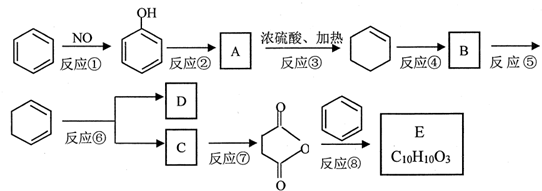
已知:①CH3CH=CHCH3能被氧化成乙酸;
②
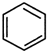 +(CH3CO)2O→
+(CH3CO)2O→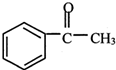 +CH3COOH
+CH3COOH(1)以上合成路线中,属于氧化反应的有:反应⑥和反应①(填反应编号);反应⑤的反应条件是氢氧化钠醇溶液、加热.
(2)写出结构简式A
 ; B
; B
(3)己知C的分子式为C4H6O4,则D的结构简式为HOOCCOOH;分离C和D的方法是蒸馏.
(4)不能由
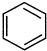 直接制取
直接制取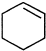 ,原因是苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷.
,原因是苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷.(5)写出反应⑧的化学方程式
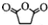 +
+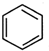 →
→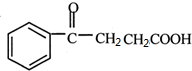 .
.
分析 根据各物质转化关系, 发生氧化反应得
发生氧化反应得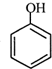 ,
, 与氢气发生加成反应得A为
与氢气发生加成反应得A为 ,A在浓硫酸作用下发生消去反应得
,A在浓硫酸作用下发生消去反应得 ,
, 与溴加成得B为
与溴加成得B为 ,B发和消去反应得
,B发和消去反应得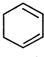 ,
, 发生信息①的氧化反应得HOOCCOOH和HOOCCH2CH2COOH,C的分子式为C4H6O4,C发生脱水反应生成
发生信息①的氧化反应得HOOCCOOH和HOOCCH2CH2COOH,C的分子式为C4H6O4,C发生脱水反应生成 ,所以C为HOOCCH2CH2COOH,D为HOOCCOOH,丁二酸酐发生信息②中的取代反应生成E为
,所以C为HOOCCH2CH2COOH,D为HOOCCOOH,丁二酸酐发生信息②中的取代反应生成E为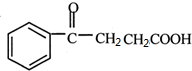 ,据此答题.
,据此答题.
解答 解:根据各物质转化关系, 发生氧化反应得
发生氧化反应得 ,
, 与氢气发生加成反应得A为
与氢气发生加成反应得A为 ,A在浓硫酸作用下发生消去反应得
,A在浓硫酸作用下发生消去反应得 ,
, 与溴加成得B为
与溴加成得B为 ,B发和消去反应得
,B发和消去反应得 ,
, 发生信息①的氧化反应得HOOCCOOH和HOOCCH2CH2COOH,C的分子式为C4H6O4,C发生脱水反应生成
发生信息①的氧化反应得HOOCCOOH和HOOCCH2CH2COOH,C的分子式为C4H6O4,C发生脱水反应生成 ,所以C为HOOCCH2CH2COOH,D为HOOCCOOH,丁二酸酐发生信息②中的取代反应生成E为
,所以C为HOOCCH2CH2COOH,D为HOOCCOOH,丁二酸酐发生信息②中的取代反应生成E为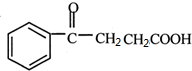 ,
,
(1)根据上面的分析可知,以上合成路线中,属于氧化反应的有:反应⑥和反应①,反应⑤为卤代烃的消去反应,所以反应条件是氢氧化钠醇溶液、加热,
故答案为:①;氢氧化钠醇溶液、加热;
(2)根据上面的分析可知,A为 ,B为
,B为 ,
,
故答案为: ;
; ;
;
(3)根据上面的分析可知,D为HOOCCOOH,C和D都是二元羧酸,它们能互溶但沸点不同,所以分离C和D的方法是蒸馏,
故答案为:HOOCCOOH;蒸馏;
(4)由于苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷,所以不能由 直接制取
直接制取 ,
,
故答案为:苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷;
(5)反应⑧的化学方程式为 +
+ →
→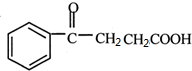 ,
,
故答案为: +
+ →
→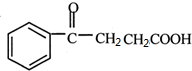 .
.
点评 本题考查有机物推断,注意运用正向推断、逆向推断及题给信息相结合进行分析解答,难度中等.

练习册系列答案
相关题目
6.铜锡合金,又称青铜,含锡量为$\frac{1}{4}$~$\frac{1}{7}$(质量比)的青铜被称作钟青铜.有一铜锡合金样品,可通过至少增加a g锡或至少减少b g铜恰好使其成为钟青铜,增加ag锡后的质量是减少bg铜后质量的2倍.则原铜锡合金样品中铜锡的质量之比为( )
| A. | 7:17 | B. | 3:2 | C. | 12:1 | D. | 7:1 |
7.下列物质应用过程中,没有发生氧化还原反应的是( )
| A. | 铝热剂用于焊接钢轨 | B. | 过氧化钠用于呼吸面具供氧 | ||
| C. | 湿润红色石蕊试纸检验氨气 | D. | 湿润的淀粉碘化钾试纸检验氯气 |
4.取0.5mL某溶液,要将其中的Fe3+和Cu2+先分离再检验,适宜的方法是( )
| A. | 纸上层析法 | B. | 萃取分液法 | C. | 结晶法 | D. | 蒸馏法 |
11.有v1mL pH=9的氨水(A)和v2mL pH=10的氨水(B),v3mL pH=10的NaOH溶液(C),它们能中和同量的盐酸.以下叙述正确的是( )
| A. | v1>10v2 | |
| B. | 加少量水稀释,氨水中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$都减小 | |
| C. | v2=v3 | |
| D. | 中和热A=B=C |
8.某未知溶液可能含Na+、NH4+、Fe2+、I-、Cl-、CO32-、SO32-.将该溶液加少量新制氯水,溶液变黄色.再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象.下列推断合理的是( )
| A. | 一定存在Fe2+、Na+、Cl- | B. | 一定不存在I-、SO32- | ||
| C. | 一定呈碱性 | D. | 一定存在NH4+ |
 已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)
已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)