题目内容
5.工业上从含硒的废液中提取硒的方法之一是:用硫酸和硝酸处理废料,获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸(2HCl+H2SeO4=H2SeO3+Cl2↑+H2O),在亚硒酸溶液中通入SO2,有单质硒析出.下列说法错误的是( )| A. | 氧化性:H2SeO4>Cl2;H2SeO3>H2SO4 | |
| B. | 酸性:H2SO4>H2SeO4>H2SeO3 | |
| C. | 析出l mol硒需要消耗标准状况下22.4 L SO2 | |
| D. | 亚硒酸理论上既有氧化性,又有还原性,但还原性不及亚硫酸 |
分析 该反应中Cl元素化合价由-1价变为0价、Se元素化合价由+6价变为+4价,所以HCl是还原剂、H2SeO4是氧化剂、氯气是氧化产物、H2SeO3是还原产物;在亚硒酸溶液中通入SO2,有单质硒析出,则二氧化硫失电子作还原剂、H2SeO3是氧化剂,硫酸是氧化产物,
A.氧化剂的氧化性大于氧化产物的氧化性;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;同一种元素含氧酸中,中心元素化合价越高其酸性越强;
C.根据Se和二氧化硫之间的关系式计算;
D.处于中间价态的元素既有氧化性又有还原性.
解答 解:A.该反应中Cl元素化合价由-1价变为0价、Se元素化合价由+6价变为+4价,所以HCl是还原剂、H2SeO4是氧化剂、氯气是氧化产物、H2SeO3是还原产物;在亚硒酸溶液中通入SO2,有单质硒析出,则二氧化硫失电子作还原剂、H2SeO3是氧化剂,硫酸是氧化产物,所以氧化性:H2SeO4>Cl2;H2SeO3>H2SO4,故A正确;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;同一种元素含氧酸中,中心元素化合价越高其酸性越强,非金属性S>Se,所以酸性:H2SO4>H2SeO4>H2SeO3,故B正确;
C.将二氧化硫通入亚硒酸溶液中出现单质硒的沉淀,反应中Se元素化合价由+4价降低到0价,S元素化合价由+4价升高到+6价,则析出1mol硒要用H2SeO31mol,SO22mol,即标准状况下44.8L,故C错误;
D.处于中间价态的元素既有氧化性又有还原性,亚硒酸中Se元素处于中间价态,所以理论上既有氧化性,又有还原性,亚硫酸还原性和二氧化硫相似,所以但还原性不及亚硫酸,故D正确;
故选C.
点评 本题考查氧化还原反应,侧重考查基本概念、基本计算,明确氧化还原反应中元素化合价变化是解本题关键,易错选项是C.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案| A. | 饱和氯水中Cl-、NO3-、Na+、SO32-可以大量存在 | |
| B. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| C. | 向无色溶液中滴加氯水和CCl4,振荡,静置,下层溶液显紫色,说明原溶液中有I- | |
| D. | SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO32-+2I-+4H+ |
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 等体积、等物质的量浓度的氢氧化钙溶液与稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
| A. | Li | B. | Na | C. | K | D. | Rb |
| A. | 通过测同温同浓度下的Na2CO3和Na2SO3水溶液的pH可以确定碳和硫两元素非金属性强弱 | |
| B. | 苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大 | |
| C. | Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性,后者表现出漂白性 | |
| D. | 总质量一定时,甲醛和乙酸无论按什么比例混合,完全燃烧消耗氧气量或生成CO2量不变 |
| A. | 吸热反应的发生都需要加热,吸热反应都没有利用价值 | |
| B. | 若某反应正向进行时为放热反应,则该反应逆向进行时必为吸热反应 | |
| C. | 放热反应放出热量的多少与反应物的质量和状态有关 | |
| D. | 不管是吸热反应还是放热反应,升高温度,反应速率均增大 |
 羟基
羟基 羰基
羰基 酯基
酯基 醛基
醛基 羧基.
羧基. ;碳元素的氢化物除CH4外,还有C2H6;氮元素的氢化物除NH3外,还有含2个氮原子的分子的化学式为N2H4,其沸点比氨气高(填“高”或“低”),该氢化物与足量盐酸反应的化学反应方程式为N2H4+2HCl=N2H6Cl2.
;碳元素的氢化物除CH4外,还有C2H6;氮元素的氢化物除NH3外,还有含2个氮原子的分子的化学式为N2H4,其沸点比氨气高(填“高”或“低”),该氢化物与足量盐酸反应的化学反应方程式为N2H4+2HCl=N2H6Cl2.
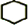 ,名称是环己烷.
,名称是环己烷. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$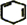 +2NaBr+2H2O.
+2NaBr+2H2O.