题目内容
15.下列有关放热反应、吸热反应的说法不正确的是( )| A. | 吸热反应的发生都需要加热,吸热反应都没有利用价值 | |
| B. | 若某反应正向进行时为放热反应,则该反应逆向进行时必为吸热反应 | |
| C. | 放热反应放出热量的多少与反应物的质量和状态有关 | |
| D. | 不管是吸热反应还是放热反应,升高温度,反应速率均增大 |
分析 A.吸热反应与条件无关,吸热反应有其利用价值,可以从生产应用中分析判断;
B.根据正逆反应的焓变数值相等符号相反判断;
C.反应放出热量的多少与反应物的用量、状态有关;
D.升高温度,无论反应是吸热还是放热反应,反应速率都会加快
解答 解:A.吸热反应与条件无关,例如氯化铵和氢氧化钡晶体反应就不需要加热;吸热反应有其利用价值,如炼铁过程中还原剂的生成虽然是吸热反应,但对炼铁过程是必须的,所以吸热反应有其利用价值,故A错误;
B.因为正逆反应的焓变数值相等符号相反,所以若某反应正向进行时为放热反应,则该反应逆向进行时必为吸热反应,故B正确;
C.因反应物的用量、状态不同,该反应的热效应也不同,所以化学反应放出热量的多少与反应物的用量、状态有关,故C正确;
D.温度升高,正逆反应速率都会加快,与反应吸热放热无关,故D正确.
故选A.
点评 本题考查吸放热反应与能量之间的关系以及温度对化学反应速率影响,本题注重了基础知识考查,难度不大.

练习册系列答案
相关题目
5.工业上从含硒的废液中提取硒的方法之一是:用硫酸和硝酸处理废料,获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸(2HCl+H2SeO4=H2SeO3+Cl2↑+H2O),在亚硒酸溶液中通入SO2,有单质硒析出.下列说法错误的是( )
| A. | 氧化性:H2SeO4>Cl2;H2SeO3>H2SO4 | |
| B. | 酸性:H2SO4>H2SeO4>H2SeO3 | |
| C. | 析出l mol硒需要消耗标准状况下22.4 L SO2 | |
| D. | 亚硒酸理论上既有氧化性,又有还原性,但还原性不及亚硫酸 |
6.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )
| A. | W、Y、Z的电负性大小顺序一定是Z>Y>W | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | Y、Z形成的分子的空间构型可能是正四面体 | |
| D. | 若有WY2,则WY2分子中σ键与π键的数目之比是2:1 |
10.M+N=Y+Z为吸热反应,对这个反应的下列说法中正确的是( )
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | Z和Y的总能量一定高于M和N的总能量 |
7.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
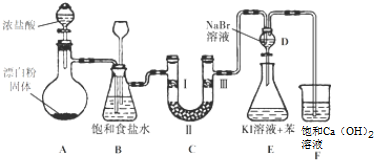
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的离子方程式:ClO-+2H++Cl-=Cl2↑++H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,该现象不能(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,离子方程式为:Cl2+2I-=I2+2Cl-(用必要的文字和离子方程式回答).
(5)此装置需要改进之处是:F原因是:氢氧化钙为微溶物,溶液中所含溶质较少,吸收氯气不充分,应改为氢氧化钠溶液吸收.

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的离子方程式:ClO-+2H++Cl-=Cl2↑++H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)此装置需要改进之处是:F原因是:氢氧化钙为微溶物,溶液中所含溶质较少,吸收氯气不充分,应改为氢氧化钠溶液吸收.
7.在298K时,2molH2燃烧生成水蒸汽放出484kJ热量,下列热化学方程式正确的是( )
| A. | 2H2+O2=2H2O,△H=-484kJ/mol | B. | H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H=+242kJ/mol | ||
| C. | 2H2(g)+O2(g)=2H2O(l),△H=-484kJ/mol | D. | H2(g)+O2(g)=H2O(g)△H=+242kJ/mol |
8.下列化合物中,只有在水溶液中才能导电的电解质是( )
| A. | H2SO4 | B. | C2H5OH | C. | NaCl | D. | NaHCO3 |
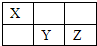 X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示.已知X、Y、Z三元素的质子数之和为40,请回答:
X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示.已知X、Y、Z三元素的质子数之和为40,请回答: .
.