题目内容
6.(1)由A、B两种气态烃组成的混合气体,对H2的相对密度为17.常温常压下,取这种混合气体10mL与80mL氧气(过量)混合,当完全燃烧后恢复到原状态时,测得气体的体积为70mL.试求:①混合气体的平均组成为(用CxHy的形式表示)C2.5H4;
②若上述两种气体按体积1:1混合时,则两种气态烃的可能组成为CH4和C4H4或C2H4和C3H4或C2H2和C3H6.
(2)具有支链的化合物X的分子式为C4H8O,X既能使Br2的四氯化碳溶液褪色,又能与Na反应.①X的结构简式是
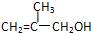 ,
,②写出与X具有相同官能团的X的所有同分异构体的结构简式:CH2=CH-CH2-CH2OH、CH2=CH-CH(OH)CH3、CH3-CH=CH-CH2OH.
分析 (1)①密度与摩尔质量成正比,混合烃对H2的相对密度为17,据此可以计算出混合烃的平均摩尔质量,然后设出混合烃的平均分子式,根据差量法计算出平均H原子数,再根据平均摩尔质量计算出含有的平均C原子数;
②根据平均分子式及两种气体按体积1:1进行讨论,得出每种体积的烃的组成;
(2)具有支链的化合物X的分子式为C4H8O,X既能使Br2的四氯化碳溶液褪色,又能与Na反应,说明含官能团羟基和碳碳双键,据此写出X的结构简式和符合条件的同分异构体.
解答 解:(1)①设混合烃的平均分子式为CxHy,密度与摩尔质量成正比,混合烃对H2的相对密度为17,则混合烃的平均摩尔质量为17g/mol×2=34g/mol,则12x+y=34,
混合烃燃烧的方程式为:CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,△n,
1 x+$\frac{y}{4}$ x 1+$\frac{y}{4}$
10mL (10+80-70)=20mL
(1+$\frac{y}{4}$):1=20mL:10mL,解得:y=4,将y=4代入12x+y=34可得x=2.5,所以混合气体的平均组成为C2.5H4,
故答案为:C2.5H4;
②混合气体的平均组成为C2.5H4,当含有甲烷时,则另一种烃分子中含有H数目为4,设另一种烃含有的C数目为x,则:$\frac{1+x}{2}$=2.5,解得:x=4,所以另一种烃为C4H4;当不含甲烷时,必须含有2个C的烃,若为C2H4,另一种烃分子中H数目必须为4,设另一种烃中含有C数目为y,则:$\frac{2+y}{2}$=2.5,解得:y=3,即另一种气态烃为C3H4;若为C2H2,设另一种烃中含有C数目为z,则$\frac{2+z}{2}$=2.5,解得z=3,设另一种烃中含有H数目为a,则:$\frac{2+a}{2}$=4,解得a=6,即另一种气态烃为C3H6,
故答案为:CH4和C4H4或C2H4和C3H4 或C2H2和C3H6;
(2)具有支链的化合物X的分子式为C4H8O,X既能使Br2的四氯化碳溶液褪色,又能与Na反应,说明含官能团羟基和碳碳双键,X的结构简式为: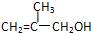 ,
,
含羟基和碳碳双键的同分异构体为:CH2=CH-CH2-CH2OH、CH2=CH-CH(OH)CH3、CH3-CH=CH-CH2OH;
故答案为: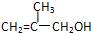 ;CH2=CH-CH2-CH2OH、CH2=CH-CH(OH)CH3、CH3-CH=CH-CH2OH.
;CH2=CH-CH2-CH2OH、CH2=CH-CH(OH)CH3、CH3-CH=CH-CH2OH.
点评 本题考查了有关混合物反应的计算,题目难度中等,明确平均摩尔质量在化学计算中的应用,(2)为难点,需要根据常见烃的分子组成特点结合平均分子式中C、H平均组成进行讨论,试题培养了学生的分析能力及化学计算能力.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | ||
| C. | 铝粉与盐酸的反应 | D. | 氧化钙溶于水 |
| A. | V(C):V(B)=2:3 | |
| B. | 单位时间生成nmolA,同时生成3nmolB | |
| C. | A、B、C的体积分数不再变化 | |
| D. | A、B、C的分子数比为1:3:2 |
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
| A. | 离子半径大小:Y2->M2->R3+ | |
| B. | Y与M组成的化合物是形成酸雨的原因之一 | |
| C. | 将YM2通入BaCl2溶液中有大量白色沉淀产生 | |
| D. | X的最高价氧化物的水化物碱性大于R最高价氧化物的水化物碱性 |
| A. |  | B. |  | C. | 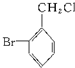 | D. | 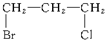 |
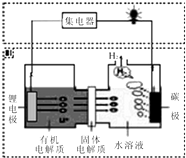 近几年科学家发明的一种新型可控电池--锂水电池,工作原理如图所示.下列有关说法不正确的是( )
近几年科学家发明的一种新型可控电池--锂水电池,工作原理如图所示.下列有关说法不正确的是( )| A. | 碳极发生的反应是:2H2O+2e-=H2↑+2OH - | |
| B. | 有机电解质和水溶液不可以互换区域 | |
| C. | 标况下产生22.4L的氢气时,正极消耗锂的质量为14g | |
| D. | 该装置不仅可提供电能,还可得到清洁的氢气 |
| A. | 该溶液中,K+、Fe2+、I-、Br-可以大量共存 | |
| B. | 用该溶液中溶解一定量铜粉,向所得溶液中再加入铁粉,若溶液中有Cu2+,则一定没有固体析出 | |
| C. | 将该溶液蒸干,得到的固体中混有氢氧化铁 | |
| D. | 100mL 0.1 mol/L该溶液和足量的Zn充分反应,生成1.12 gFe |