题目内容
5. 回答下列问题.
回答下列问题.(1)如图,某温度(t℃)时水的图象如下,a点离子积KW=1.0×10-12mol2•L-2;该温度下,pH=12的NaOH与pH=2的H2SO4等体积混合,溶液显碱性.
(2)25℃时,向0.1mol•L-1氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH减小,NH+4的物质的量浓度增大.(填增大、减小或不变)
(3)体积相等的稀NaOH和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则该溶液显中性(填“酸性”、“碱性”、“中性”),则混合前c(NaOH)<C(CH3COOH)(填“>”、“<”或“=”).
(4)常温时,Fe(OH)3的Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留在溶液中的c(Fe3+)<10-5mol•L-1),则溶液的pH最小为3.
(5)用可溶性碳酸盐,可以浸取CaSO4固体,则溶液浸取过程中会发生反应:
CaSO4(s)+CO2-3(aq)?CaCO3(s)+SO2-4(aq).
已知298K时,KSP(CaCO3)=2.80×10-9,KSP(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为1.75×104(计算结果保留三位有效数字).
分析 (1)根据离子积常数=c(H+)×c(OH-)进行计算;根据水的离子积计算酸碱溶液中氢离子、氢氧根离子浓度,根据硫酸中氢离子与氢氧化钠中氢氧根离子的物质的量判断碱过量;
(2)向氨水中加入氯化铵,铵根离子浓度的抑制一水合氨电离;
(3)根据电荷守恒判断,醋酸钠溶液呈碱性,要使醋酸和氢氧化钠的混合溶液呈中性,则醋酸应该稍微过量;
(4)依据氢氧化铁的溶度积常数和Fe3+沉淀完全的浓度为c(Fe3+)<10-5mol•L-1,计算氢氧根离子浓度得到溶液最小pH;
(5)以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq)平衡常数概念写出计算式,依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算分析;
解答 解:(1)根据图知,当c(H+)=10-6 mol/L,c(OH-)=10-6 mol/L,由离子积常数=c(H+)×c(OH-)=10-6.×10-6=10-12,pH=2的H2SO4溶液中c(H+)=0.01mol/L,pH=12的NaOH中c(OH-)=$\frac{1{0}^{-12}}{1{0}^{-12}}$=1mol/L,等体积混合时碱过量,溶液呈碱性,
故答案为:1.0×10-12;碱;
(2)一水合氨为弱电解质,溶液中存在电离平衡NH3•H2O?NH4++OH-,向氨水中加入氯化铵时,溶液中铵根离子浓度增大,抑制一水合氨电离,溶液中氢氧根离子浓度减小,则pH减小,
故答案为:减小;增大;
(3)溶液中存在电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),c(Na+)=c(CH3COO-),所以c(OH-)=c(H+),所以溶液呈中性;醋酸钠溶液呈碱性,要使醋酸和氢氧化钠的混合溶液呈中性,则醋酸应该稍微过量,因为二者的体积相等,所以醋酸的浓度大于氢氧化钠,
故答案为:中性,<;
(4)常温时,Fe(OH)3的Ksp=1×10-38,要使溶液中的Fe3+沉淀完全,残留在溶液中的c(Fe3+)<10-5mol•L-1;Ksp=c(Fe3+)c3(OH-)=10-5×c3(OH-)=1×10-38 c(OH-)=10-11mol/L,c(H+)=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3mol/L,溶液PH=3;
故答案为:3;
(5)溶浸过程中会发生:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq),CaCO3(s)=Ca2++CO32-;CaSO4(s)=Ca2++SO42-;依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算,反应的平衡常数K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=$\frac{Ksp(CaS{O}_{4})}{Ksp(CaC{O}_{3})}$=$\frac{4.90×1{0}^{-5}}{2.80×1{0}^{-9}}$=1.75×104,
故答案为:1.75×104.
点评 本题考查了酸碱混合溶液定性判断、盐类水解、溶度积常数的计算等知识点,明确物质的性质是解本题关键,再结合盐类水解的影响因素结合电荷守恒来分析解答,题目难度中等,难点是平衡常数的计算应用,溶度积的计算分析.

 阅读快车系列答案
阅读快车系列答案(1)钪(Sc)元素的原子核外电子排布式为1s22s22p63s23p63d14s2.钬(Ho)的基态原子电子排布式为[Xe]4f116s2,一个基态钬原子所含的未成对电子数为3.
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价.请根据下表中的电离能数,判断表中最可能有+4价的元素是Ce.
几种稀土元素的电离能(单位:kJ•mol-1)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.
ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点则PrO2(二氧化镨)的晶胞中有9个氧原子.
(6)Ce(铈)单质为面心立方晶体,其晶胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12.列式表示Ce(铈)单质的密度为$\frac{4×140}{6.02×1{0}^{23}×(516×1{0}^{-10})^{3}}$g•cm-3(不必计算出结果).

| A. | 反应过程可表示为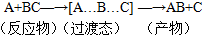 | |
| B. | E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能 | |
| C. | 此图中逆反应的热效应△H=E1-E2,为吸热反应 | |
| D. | 此图中正反应的热效应为△H=E1-E2,且E2>E1,所以正反应为放热反应 |
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. |  +Br2$\stackrel{催化剂}{→}$ +Br2$\stackrel{催化剂}{→}$ +H2O +H2O | |
| C. | 2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O | |
| D. | CH2═CH2+HCl→CH3CH2Cl |
| A. | 氯气溶解于水:Cl2+H2O═HClO+Cl-+H+ | |
| B. | 沸水中滴入饱和FeCl3溶液,溶液呈红褐色:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| C. | 醋酸钠溶液显碱性:CH3COO-+H2O═CH3COOH+OH-. | |
| D. | 久置的H2S 溶液变浑浊:2S2-+O2+4H+═2S↓+2H2O |