题目内容
10.Ⅰ.为证明Fe3+具有较强的氧化性,甲同学做了如下实验:将Cu片放入0.5mol/L Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较强氧化性的结论.乙同学提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性条件下NO3-也能氧化Cu”,并设计实验进行探究.已知:
| 水解反应 | 平衡常数(K) |
| Fe3++3H2O?Fe(OH)3+3H+ | 7.9×10-4 |
| Fe2++2H2O?Fe(OH)2+2H+ | 3.2×10-10 |
| Cu2++2H2O?Cu(OH)2+2H+ | 3.2×10-7 |
试剂:0.5mol/L Fe(NO3)3溶液、Cu片、精密pH试纸(0.5~5.0)、5mol/L硝酸钠溶液、0.5mol/L硝酸钠溶液、0.1mol/L稀盐酸、蒸馏水.
方案测定硝酸铁溶液的pH,再用硝酸钠溶液和稀盐酸配制成与硝酸铁溶液PH相同、硝酸根离子浓度相同的溶液,将铜片加入到该溶液中,观察二者是否反应.
(2)丙同学分别实施了甲、乙两位同学的实验方案,并在实验过程中用pH计监测溶液pH的变化,实验记录如下.
| 实验内容 | 实验现象 |
| 甲同学的实验方案 | 溶液逐渐变成蓝绿色,pH略有上升 |
| 乙同学的实验方案 | 无明显现象,pH没有明显变化. |
②导致实验过程中溶液pH略有上升的可能原因是Fe3+变为Cu2+和Fe2+,水解能力下降.
③解释乙同学的实验现象在此酸性条件下NO3-不能氧化Cu.
(3)请你设计更简便可行的实验方案,帮助甲同学达到实验目的将铜片放入0.5mol/L氯化铁溶液中.
Ⅱ.聚合氯化铁铝(简称PAFC),其化学通式为[FexAly(OH)aClb•zH2O]m.某同学为测定其组成,进行如下实验:①准确称取4.505 0g样品,溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到2.330 0g固体.②另准确称取等质量样品溶于水,在溶液中加入适量Zn粉和稀硫酸,将Fe3+完全还原为Fe2+.用0.100 0mol•L-1标准KMnO4溶液滴定Fe2+,消耗标准溶液的体积为20.00mL.③另准确称取等质量样品,用硝酸溶解后,加入足量AgNO3溶液,得到4.305 0g白色沉淀.(相对原子质量或式量:Fe-56 Al-27 Cl-35.5 O-16 H-1 Fe2O3-160 Al2O3-102 AgCl-143.5 H2O-18)
(4)若滴定管在使用前未用KMnO4标准溶液润洗,测得的Al3+含量将偏低(填“偏高”“偏低”或“不变”).
(5)通过计算确定PAFC的化学式[FeAl3(OH)9Cl3•3H2O]m或FeAl3(OH)9Cl3•3H2O(写出计算过程;不要求写出反应方程式;m为聚合度,不必求出).
分析 (1)铁离子水解呈酸性,如验证乙同学的看法是否正确,可测定0.5mol/L Fe(NO3)3溶液的pH,然后在硝酸钠溶液中滴加盐酸,与硝酸铁溶液PH相同、硝酸根离子浓度相同,加入铜观察是否反应;
(2)甲同学的实验方案中溶液逐渐变成蓝绿色,pH略有上升,说明铁离子氧化铜,注意比较离子水解的程度;乙同学的实验方案无明显现象,pH没有明显变化,说明不反应;
(3)如证明铁离子氧化铜,可排除硝酸根离子的影响,应用其它可溶性铁盐;
(4)若滴定管在使用前未用标准溶液润洗,相当于用的标准液的浓度偏小,所以用到的体积偏高,测得待测液中亚铁离子的浓度偏大,即铁离子偏大;
(5)①称取样品溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到2.3300g固体是氧化铝和氧化铁;
②另准确称取等质量样品溶于水,在溶液中加入适量Zn粉和稀硫酸,将Fe3+完全还原为Fe2+,用0.1000mol•L-1标准KMnO4溶液滴定Fe2+,消耗标准溶液的体积为20.00mL,根据KMnO4~5Fe2+~5Fe3+,可以计算铁离子的量,根据①结合元素守恒计算Al元素的含量;
③另准确称取等质量样品,用硝酸溶解后,加入足量AgNO3溶液,得到4.3050g白色沉淀即AgCl沉淀,可以计算Cl元素的量.
解答 解:(1)铁离子水解呈酸性,如验证乙同学的看法是否正确,可测定0.5mol/L Fe(NO3)3溶液的pH,然后在硝酸钠溶液中滴加盐酸,与硝酸铁溶液PH相同、硝酸根离子浓度相同,做法是测定硝酸铁溶液的pH,再用硝酸钠溶液和稀盐酸配制成与硝酸铁溶液PH相同、硝酸根离子浓度相同的溶液,将铜片加入到该溶液中,观察二者是否反应,
故答案为:测定硝酸铁溶液的pH,再用硝酸钠溶液和稀盐酸配制成与硝酸铁溶液PH相同、硝酸根离子浓度相同的溶液,将铜片加入到该溶液中,观察二者是否反应;
(2)①甲同学的实验方案中溶液逐渐变成蓝绿色,pH略有上升,说明铁离子氧化铜,反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,
故答案为:Cu+2Fe3+=Cu2++2Fe2+;
②因Fe3+ 变为Cu2+和Fe2+,水解能力下降,导致实验过程中溶液pH略有上升,
故答案为:Fe3+变为Cu2+和Fe2+,水解能力下降;
③乙同学的实验方案无明显现象,pH没有明显变化,说明不反应,
故答案为:在此酸性条件下NO3-不能氧化Cu;
(3)如证明铁离子氧化铜,可排除硝酸根离子的影响,应用其它可溶性铁盐,将铜片放入0.5mol/L氯化铁溶液中,
故答案为:将铜片放入0.5mol/L氯化铁溶液中;
(4)若滴定管在使用前未用标准溶液润洗,相当于用的标准液的浓度偏小,所以用到的体积偏高,测得待测液中亚铁离子的浓度偏大,即铁离子偏大,测得的Al3+含量将偏低,
故答案为:偏低;
(5)①称取样品溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到2.3300g固体是氧化铝和氧化铁;
②另准确称取等质量样品溶于水,在溶液中加入适量Zn粉和稀硫酸,将Fe3+完全还原为Fe2+,用0.1000mol•L-1标准KMnO4溶液滴定Fe2+,消耗标准溶液的体积为20.00mL,根据KMnO4~5Fe2+~5Fe3+,则Fe3+的物质的量是0.5×20×10-3mol=0.01mol,氧化铁的质量是:0.01mol×0.5×160g/mol=0.8g,氧化铝质量为:2.33g-0.8g=1.53g,所以Al3+的物质的量是:n(Al3+)=2n(Al2O3)=2×$\frac{1.53g}{102g/mol}$=0.03mol,
③另准确称取等质量样品,用硝酸溶解后,加入足量AgNO3溶液,得到4.3050g白色沉淀即AgCl沉淀,则n(Cl-)=n(AgCl)=$\frac{4.3050g}{143.5g/mol}$=0.03mol,
根据电荷守恒:3n(Fe3+)+3n(Al3+)=n(Cl-)+n(OH-),所以n(OH-)=0.01mol×3+0.03mol×3-0.03mol=0.09mol,
n(H2O)=$\frac{4.5050-m(F{e}^{3+})-m(A{l}^{3+})-m(C{l}^{-})-m(O{H}^{-})}{18g/mol}$=0.03mol,
综上可知:n(Fe3+):n(Al3+):n(Cl-):n(OH-):n(H2O)=1:3:3:9:3,
所以PAFC的化学式为:[FeAl3(OH)9Cl3•3H2O]m或FeAl3(OH)9Cl3•3H2O,
故答案为:[FeAl3(OH)9Cl3•3H2O]m或FeAl3(OH)9Cl3•3H2O.
点评 本题考查了性质实验方案的设计,题目难度较大,涉及实验方案的设计与评价、中和滴定、复杂化学式计算等知识,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验、化学计算能力,(5)为易错点,注意掌握复杂化学式的确定方法.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 油脂在空气中完全燃烧转化为水和二氧化碳 | |
| B. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 | |
| C. | 在水溶液里,乙酸分子中的-CH3可以电离出H+ | |
| D. | 医学上了利用银镜反应来检验患者尿液中葡萄糖含量是否偏高 |
一定条件下反应:2A(g)+B(g) 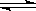 3C(g) ΔH<0,在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
3C(g) ΔH<0,在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | A的浓度 | 平衡常数K |
B | 温度 | 混合气体的密度 |
C | B的物质的量 | A的转化率 |
D | 催化剂的质量 | C的体积分数 |

已知几种氢氧化物开始沉淀和完全沉淀的pH如下表所示
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
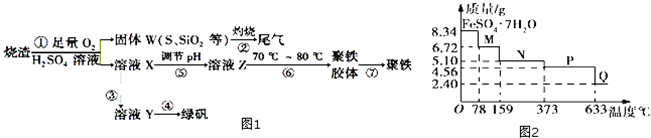
(1)用2mol/L H2SO4溶液溶解草酸亚铁样品而不用蒸馏水直接溶解的原因是防止Fe2+水解加热至70℃左右,立即用KMnO4溶液滴定至终点.发生反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O和MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
(2)保温放置30min的目的是使反应更完全
(3)证明反应Ⅰ完全的实验操作或现象为溶液呈紫红色,取少许紫红色溶液于试管中,滴加KSCN溶液,溶液颜色无明显变化
(4)已知常温下Fe(OH)3的Ksp=1.1×10-36,废液中c(Fe3+)=1.1×10-6mol•L-1.
(5)灼烧充分的标志是连续两次灼烧、冷却、称量所得质量差不超过0.1g
(6)样品中FeC2O4的含量为72%.
| A. | 用酸性高锰酸钾溶液鉴别乙烷与乙烯 | |
| B. | 向蔗糖溶液中加入稀硫酸,加热,冷却后加入新制Cu(OH)2检验水解产物 | |
| C. | 用饱和Na2CO3溶液鉴别乙酸、乙醇、硝基苯 | |
| D. | 利用燃烧的方法鉴别羊毛和棉花 |
 2NH3(g) ΔH=-92.4 kJ·m
2NH3(g) ΔH=-92.4 kJ·m ol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是
ol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是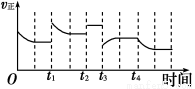
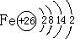 ,
,