题目内容
【题目】将![]() 持续通入下列八种饱和溶液:
持续通入下列八种饱和溶液:![]()
![]()
![]()
![]()
![]()
![]() 和NaCl
和NaCl![]() ,最终能得到沉淀、浊液或析出晶体的是
,最终能得到沉淀、浊液或析出晶体的是
A.②⑤⑧B.⑤⑥⑧C.①②③④⑦D.②③④⑧
【答案】C
【解析】
①过量的![]() 通入饱和
通入饱和![]() 溶液中发生反应生成碳酸氢钠,碳酸氢钠溶解性小于碳酸钠,所以有晶体碳酸氢钠析出,故正确;
溶液中发生反应生成碳酸氢钠,碳酸氢钠溶解性小于碳酸钠,所以有晶体碳酸氢钠析出,故正确;
②碳酸的酸性强于硅酸,向硅酸钾溶液中通入二氧化碳生成硅酸沉淀,故正确;
③NaAlO2溶液通入过量的二氧化碳,可生成氢氧化铝沉淀,故正确;
④碳酸的酸性强于苯酚,二氧化碳通入苯酚钠溶液生成苯酚沉淀,故正确;
⑤碳酸的酸性强于次氯酸,过量二氧化碳能够与次氯酸钙反应生成碳酸氢钙,碳酸氢钙易溶于水,故错误;
⑥碳酸的酸性弱于盐酸,与氯化钙不反应,不会产生沉淀,故错误;
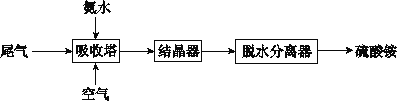
⑦可生成碳酸氢钠和氯化铵,为侯氏制碱法原理,发生反应:![]() ,所以有
,所以有![]() 晶体析出,故正确;
晶体析出,故正确;
⑧过量的![]() 与
与![]() 反应生成碳酸氢钙和水,碳酸氢钙溶于水,故错误;
反应生成碳酸氢钙和水,碳酸氢钙溶于水,故错误;
①②③④⑦正确,故选C。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案【题目】下列生产或实验事实引出的相应结论不正确的是( )
选项 | 事实 | 结论 |
A | 工业制硫酸中,在矿石处理阶段,将矿石粉碎再煅烧 | 增大反应物的接触面积,加快化学反应速率 |
B | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入MnO2,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
C | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
D | 一定条件下:H2(g)+I2(g) | c(I2)增大,I2物质的量增多 |
A. A B. B C. C D. D
【题目】某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用10mL H2O2制取150mLO2所需的时间(秒)
| 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
无催化剂、加热 | 360 | 480 | 540 | 720 |
MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
①该研究小组在设计方案时。考虑了浓度、___________、____________等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_______________________。
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%(密度为1.0g/cm3)的双氧水中,并用带火星的木条测试。测定结果如下:
实验 序号 | 催化剂(MnO2) | 操作 情况 | 观察结果 | 反应完成 所需的时间 |
A | 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 5span>分钟 |
B | 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
① 写出H2O2发生分解的化学反应方程式________________。求出实验A中H2O2在5分钟内的平均反应速率________________。(结果保留小数点后两位数字)
② 实验结果说明催化剂作用的大小与____________________有关。