题目内容
【题目】将18.0 g由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了5.4 g。另取等质量的合金溶于过量稀HNO3中,生成了8.96 L NO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则沉淀的质量为
A.22.8 gB.25.4 gC.33.2gD.无法计算
【答案】A
【解析】
将18.0克由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,只有铝参与反应,则合金质量减少的5.4克为Al,物质的量为![]() ;将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Cu2+离子,根据电子守恒,金属共失去电子的物质的量为
;将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Cu2+离子,根据电子守恒,金属共失去电子的物质的量为![]() ,其中0.2mol铝完全反应失去0.6mol电子,则Cu、Fe完全反应失去电子为1.2mol-0.6mol=0.6mol,反应中Cu、Fe失去电子的物质的量等于生成碱的氢氧根离子的物质的量,则n(OH-)=0.6mol,从金属单质转化为其氢氧化物,增加的是氢氧根离子的质量,所以反应后沉淀的质量(包括氢氧化铝)等于18.0g+0.6mol×17g/mol=28.2g,但是加入过量氢氧化钠后,不会生成氢氧化铝沉淀,开始合金质量减少了5.4g,所以反应后氢氧化铜、氢氧化铁的质量为28.2g-5.4g=22.8g,答案选A。
,其中0.2mol铝完全反应失去0.6mol电子,则Cu、Fe完全反应失去电子为1.2mol-0.6mol=0.6mol,反应中Cu、Fe失去电子的物质的量等于生成碱的氢氧根离子的物质的量,则n(OH-)=0.6mol,从金属单质转化为其氢氧化物,增加的是氢氧根离子的质量,所以反应后沉淀的质量(包括氢氧化铝)等于18.0g+0.6mol×17g/mol=28.2g,但是加入过量氢氧化钠后,不会生成氢氧化铝沉淀,开始合金质量减少了5.4g,所以反应后氢氧化铜、氢氧化铁的质量为28.2g-5.4g=22.8g,答案选A。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】H2是一种重要的清洁能源。
(1)已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.1kJmol-1
CO2(g)+H2(g) ΔH3=-41.1kJmol-1
H2还原 CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
A.高温 B.低温 C.任何温度条件下
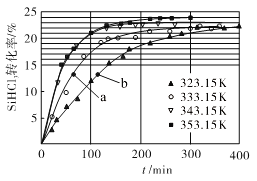
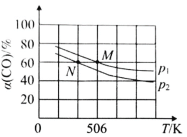
(2)恒温恒压下,在容积可变的密闭容器中加入 1molCO和2.2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
(3)若反应 CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是____(填字母);
C.混合气体的相对分子质量保持不变 D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=___(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=___kPamin-1。