题目内容
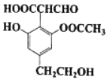
【题目】某有机物的结构简式如图所示,下列关于该有机物的性质说法正确的是( )
A.可与银氨溶液反应,不与![]() 溶液反应显色
溶液反应显色
B.可以与![]() 反应,1 mol该物质最多消耗
反应,1 mol该物质最多消耗![]()
C.1 mol该物质与足量金属Na反应,最多产生![]()
D.1 mol物质与NaOH溶液反应,最多消耗3 mol NaOH
【答案】C
【解析】
A.该物质中含![]() 可发生银镜反应,含酚羟基可与
可发生银镜反应,含酚羟基可与![]() 溶液反应显色,A项错误;
溶液反应显色,A项错误;
B.该物质分子结构中的苯环、![]() 可以与氢气发生加成反应,因此1mol该物质最多消耗
可以与氢气发生加成反应,因此1mol该物质最多消耗![]() ,B项错误;
,B项错误;
C.该物质分子结构中的![]() 、
、![]() 均与Na反应生成氢气,则1mol该物质与足量金属Na反应,最多产生
均与Na反应生成氢气,则1mol该物质与足量金属Na反应,最多产生![]() ,C项正确;
,C项正确;
D.该物质分子结构中的![]() 、
、![]() 、酚羟基及水解生成的酚羟基均可与NaOH反应,则1mol该物质与NaOH溶液反应,最多消耗4molNaOH,D项错误;
、酚羟基及水解生成的酚羟基均可与NaOH反应,则1mol该物质与NaOH溶液反应,最多消耗4molNaOH,D项错误;
答案选C。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目