题目内容
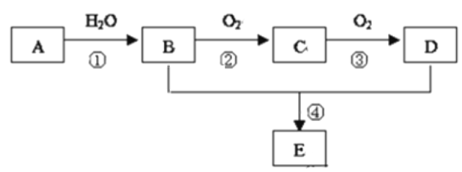
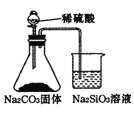
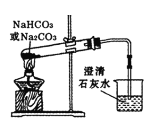
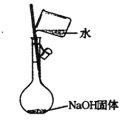
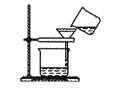
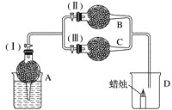
【题目】干燥管 A 中为块状白色固体,烧杯中为稀盐酸,B 中为淡黄色粉末,C 中与 B含有相同阳离子的为白色半透明结晶状的固体碱,C 的火焰反应呈黄色。并将 A、B、C 按如图所示装置连接,当打开活塞(I)(II),关闭(III)时,D 中蜡烛火焰明亮;打开活塞(I)(III)时, D 中蜡烛火焰没有明显变化;关闭活塞(I)时,A 中反应自行停止。
试根据上述实验事实,回答以下各问题:
(1)在装置B 中发生的化学反应是_______。
(2)在干燥管C 中的白色固体的俗名_____。写出 C 中发生化学反应的方程式:______。
【答案】2Na2O2+2CO2=2Na2CO3+O2 烧碱(火碱、或苛性钠都行) 2NaOH+ CO2=Na2CO3+H2O(或 NaOH+ CO2=NaHCO3)
【解析】
根据题中信息和图示,可判断装置A为产生CO2的简易启普发生器,装置B为探究Na2O2与CO2反应,由装置D 中蜡烛火焰明亮,可判断有O2生成;装置C为吸收CO2,否则D 中蜡烛火焰会熄灭,据此分析解答。
由题中信息可知,C中与 B含有相同阳离子,C 的焰色反应呈黄色,可判断C与B均含Na元素,根据B 中为淡黄色粉末,则B为Na2O2,C中与B含有相同阳离子的为白色半透明结晶状的固体碱,C为NaOH;打开活塞(I)(II),关闭(III)时,D 中蜡烛火焰明亮,一定是通入了O2,则可确定B中是Na2O2和CO2生成O2的反应;从而可知A是产生CO2的简易启普发生器,打开活塞(I)(III)时, D 中蜡烛火焰没有明显变化,则A中产生的CO2通过装置C时被C中物质吸收了,C中为NaOH,关闭活塞(I)时,A 中反应自行停止,说明A中固体不溶于水,应为碳酸钙。由上述分析可知:
(1)B中是Na2O2和CO2生成O2的反应,化学方程式为2Na2O2+2CO2=2Na2CO3+O2;答案为2Na2O2+2CO2=2Na2CO3+O2。
(2)在干燥管C 中的白色固体为NaOH,俗名为烧碱或火碱或苛性钠,C 中发生化学反应是NaOH与CO2的反应,生成碳酸钠和水或CO2过量生成碳酸氢钠,化学方程式为2NaOH+ CO2=Na2CO3+H2O或NaOH+ CO2=NaHCO3;答案为烧碱或火碱或苛性钠,2NaOH+ CO2=Na2CO3+H2O或NaOH+ CO2=NaHCO3。

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案