题目内容
(10分)工业上常用天然气作为制备 的原料。已知:
的原料。已知:
①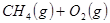


②
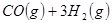

③


(1)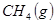 与
与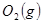 反应生成
反应生成 的热化学方程式为 。
的热化学方程式为 。
(2)向VL恒容密闭容器中充入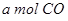 与
与 ,在不同压强下合成甲醇。
,在不同压强下合成甲醇。 的平衡转化率与温度、压强的关系如下图所示:
的平衡转化率与温度、压强的关系如下图所示:
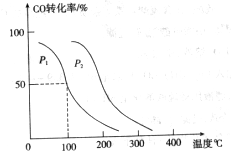
①压强
 (填“<”、“>”或“=”)
(填“<”、“>”或“=”)
②在 、
、 压强时,平衡常数为 (用含
压强时,平衡常数为 (用含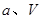 的代数式表示)。
的代数式表示)。
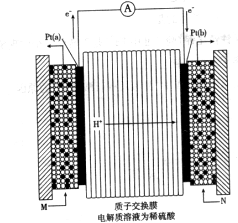
(3)下图是甲醇燃料电池(电解质溶液为稀硫酸)结构示意图, 电极通入的
电极通入的 为 ,电极反应式是 。
为 ,电极反应式是 。
若用该电池电解 溶液,当得到
溶液,当得到 铜时,参加反应的气体
铜时,参加反应的气体 的体积应为
的体积应为  (标准状况)。
(标准状况)。
 的原料。已知:
的原料。已知:①
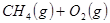


②

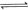

③



(1)
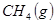 与
与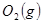 反应生成
反应生成 的热化学方程式为 。
的热化学方程式为 。(2)向VL恒容密闭容器中充入
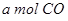 与
与 ,在不同压强下合成甲醇。
,在不同压强下合成甲醇。 的平衡转化率与温度、压强的关系如下图所示:
的平衡转化率与温度、压强的关系如下图所示:
①压强

 (填“<”、“>”或“=”)
(填“<”、“>”或“=”)②在
 、
、 压强时,平衡常数为 (用含
压强时,平衡常数为 (用含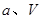 的代数式表示)。
的代数式表示)。(3)下图是甲醇燃料电池(电解质溶液为稀硫酸)结构示意图,
 电极通入的
电极通入的 为 ,电极反应式是 。
为 ,电极反应式是 。
若用该电池电解
 溶液,当得到
溶液,当得到 铜时,参加反应的气体
铜时,参加反应的气体 的体积应为
的体积应为  (标准状况)。
(标准状况)。(1)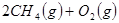
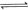
 2分
2分
(2)① < 1分
②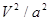 2分
2分
(3)甲醇(或 ) 1分
) 1分
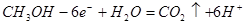 2分
2分
0.56L 2分
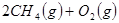
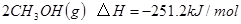 2分
2分(2)① < 1分
②
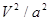 2分
2分(3)甲醇(或
 ) 1分
) 1分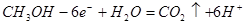 2分
2分0.56L 2分
(1)考查盖斯定律的应用。根据已知可知,①+②+③×2即得到
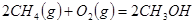 ,所以反应热是-321.5kJ/mol+250.3 kJ/mol-90 kJ/mol×2=-251.2 kJ/mol。
,所以反应热是-321.5kJ/mol+250.3 kJ/mol-90 kJ/mol×2=-251.2 kJ/mol。
(2)①反应③是体积减小的可逆反应,所以压强越大,转化率越高,因此 <
< 。
。
②根据图像可知,平衡时CO的转化率是50%,所以平衡时生成甲醇0.5amol,剩余CO和氢气分别是0.5amol和amol,因此平衡常数为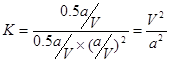 。
。
(3)根据装置图中电子的流向可知,左侧是原电池的负极,失去电子,所以左侧通入的是甲醇。应用电解质是稀硫酸,且只能允许质子通过,所以负极反应式为
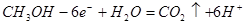 。
。
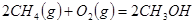 ,所以反应热是-321.5kJ/mol+250.3 kJ/mol-90 kJ/mol×2=-251.2 kJ/mol。
,所以反应热是-321.5kJ/mol+250.3 kJ/mol-90 kJ/mol×2=-251.2 kJ/mol。(2)①反应③是体积减小的可逆反应,所以压强越大,转化率越高,因此
 <
< 。
。②根据图像可知,平衡时CO的转化率是50%,所以平衡时生成甲醇0.5amol,剩余CO和氢气分别是0.5amol和amol,因此平衡常数为
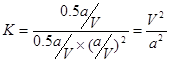 。
。(3)根据装置图中电子的流向可知,左侧是原电池的负极,失去电子,所以左侧通入的是甲醇。应用电解质是稀硫酸,且只能允许质子通过,所以负极反应式为
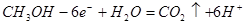 。
。
练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目

 HOCH2-CH2OH(g)+2CH3OH(g) △H =" -34" kJ/mol
HOCH2-CH2OH(g)+2CH3OH(g) △H =" -34" kJ/mol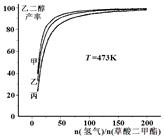
 H++OH-、HC2O4-
H++OH-、HC2O4-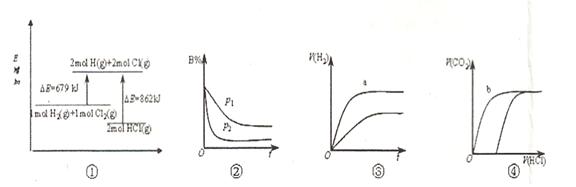
 2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化,则D一定是气体
2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化,则D一定是气体 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0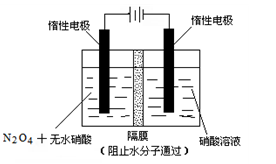
 2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1
2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1
 的焓变为ΔH = -384 kJ·mol-1
的焓变为ΔH = -384 kJ·mol-1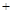 CO(g)
CO(g) CH3OH(g)
CH3OH(g)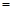 kJ;
kJ;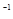 )
)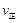 (甲醇)
(甲醇) 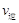 (水)(填“>”、“<”或“=”)。
(水)(填“>”、“<”或“=”)。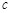 (CH3OH)
(CH3OH)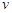 (CH3OH)
(CH3OH)
 2NH3(g) ΔH <0。400℃时,K= 0.5,某一时刻测得N2、H2和NH3三种物质物质的量分别为2mol、1mol和3mol,则该反应的v正(N2) v逆(N2)(填 “>” 、“="”" 或 “<”)
2NH3(g) ΔH <0。400℃时,K= 0.5,某一时刻测得N2、H2和NH3三种物质物质的量分别为2mol、1mol和3mol,则该反应的v正(N2) v逆(N2)(填 “>” 、“="”" 或 “<”) 浓度mol.L-1
浓度mol.L-1