题目内容
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的氢氧化物是两性氢氧化物, E的阳离子与A的阴离子核外电子层结构相同。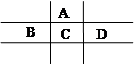
请回答下列问题:
⑴C元素在周期表中的位置为 。
⑵写出A与氢元素能形成原子物质的量之比为1∶1的化合物的结构式 ,分子中所含共价键的类型为 。
⑶比较A、C氢化物的稳定性:A C(填大于、小于或等于),原因是 。
⑷B、C、D的原子半径由大到小的顺序为(用元素符号表示) 。
⑸若将E制作成电极与石墨用导线相连,回答下列问题:
将两电极插入盛有稀H2SO4的烧杯中形成原电池,E电极为 极,写出该电池的负极的电极反应是: ;电池总反应(用离子方程式表示) 。
(15分)(1)第三周期VIA族(2分)
(2)H—O—O—H(1分);极性键、非极性键(写全得2分、不全得1分,多写为零分)。
(3)大于(1分);氧的非金属性大于硫的非金属性(2分,合理均给分)。
(4)P>S>Cl(2分,或P S Cl或Cl<S<P均给分。)
(5)负极(1分);Al-3e-=Al3+(2分) 2Al+6H+=2 Al3++3H2↑
(2分,未配平零分,元素符号写错零分,未写气体符号不扣分)
解析试题分析:设C元素的原子序数是x,则根据元素在周期表中的相对位置可知,A、B、D的原子序数分别是x-8、x-1、x+1,则x-8+x-1+x+x+1=56,解得x=16,即A是O,B是P,C是S,D是Cl元素。E的氢氧化物是两性氢氧化物,则E是Al元素。
(1)S元素的核电荷数是16,在周期表中的位置为第三周期VIA族。
(2)氧元素与氢元素形成原子物质的量之比为1∶1的化合物是双氧水,其的结构式H—O—O—H,分子中所含共价键的类型为极性键、非极性键。
(3)氧的非金属性大于硫的非金属性,非金属性越强,氢化物的稳定性越强,则水的稳定性强于H2S的稳定性。
(4)同周期自左向右原子半径逐渐减小,则B、C、D的原子半径由大到小的顺序为P>S>Cl。
(5)铝是活泼的金属,与石墨用导线连接后插入到稀硫酸中,铝是负极,失去电子,电极反应式是Al-3e-=Al3+;石墨是正极,溶液中的氢离子在正极得到电子,所以总的反应式是2Al+6H+=2 Al3++3H2↑。
考点:考查元素周期表第结构和元素周期律的应用
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。
| X | Y | Z | |
| | R | | |
| | | W | |
| | | | J |
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1) 在化合物YZ2中Y的化合价为________;Y2-与Na+的半径大小为_______________;
(2) R原子的基态电子排布式为
__________________________________________________________________________;
(3)在X、Y、Z三种元素中,第一电离能由大到小的顺序是______________________;
(4)有一种酸HX3的酸性与醋酸相近,HX3溶液与NaOH溶液反应的离子方程式为___________________________________________。
(12分)根据下列某些短周期元素中元素性质回答问题。
| | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径/10 -10m | 0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | | +3 | +4 | +5 | +7 | +1 | +5 | |
| 最低价态 | -1 | | -2 | | -4 | -3 | -1 | | -3 | -1 |
(2)元素①和⑨形成阳离子 ,其结构式为__________________。
(3)某元素R的原子半径为1.02×10 -10m ,它与钠形成Na2R2,其电子式是_________(R用元素符号表示)。
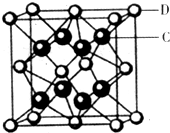
(4)元素②和⑦形成晶体的部分结构可用下图中的_________来表示(填序号)。

(5)①、③、⑨可以形成原子个数之比为4:3:2的中学常见无机化合物,该化合的水溶液显酸性的原因是_________________(用离子方程式表示),其水溶液中离子浓度由大到小的顺序是___________________。
某同学做元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验内容:(填写与实验步骤对应的实验现象的编号)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) | | | | | | |
(2)实验结论: 。
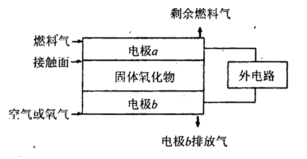
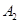 作为燃料气,则接触面上发生的反应为______________________________。
作为燃料气,则接触面上发生的反应为______________________________。 作为燃料气,则接触面上发生的反应为________________________________。
作为燃料气,则接触面上发生的反应为________________________________。