��Ŀ����
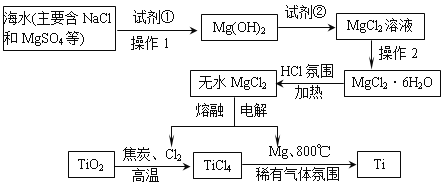
����Ŀ��Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ģ��Ӻ�ˮ����ȡ��MgCl2�Ƶ�Mg��Cl2����һ�������ý��ʯ(��Ҫ�ɷ�TiO2)ұ�������ѣ���ҵ������Ҫ�������������£�
|
�ش��������⣺
(1)��������Լ��ٺ��ܹ�����õ�Mg(OH)2�����ķ�������1�õ��IJ���������________________________________________���Լ��ڿ���ѡ��______��
(2)Ҫ�õ�MgCl2��6H2O�IJ���2������___________________________________��
(3)��ҵ��ұ�������ѵ������������̣����1�����ڸ���������ʯ(��Ҫ�ɷ�TiO2)�뽹̿�Ļ������ͨ��Cl2���õ�TiCl4��һ�ֿ�ȼ�����壬д���ⲽ��Ӧ�Ļ�ѧ����ʽ��____________________________��
(4) ��ҵ��ұ�������ѵ������������̣����2������ϡ�������Χ�ͼ��ȵ������£���þ��TiCl4��Ӧ�õ��ѣ�д���ⲽ��Ӧ�Ļ�ѧ����ʽ____________________���÷�Ӧʱϡ�������Χ��������_____________________________________���÷�Ӧ�Ľ���ұ������������____________________��
���𰸡�©�������������ձ� ���� �����ᾧ TiO2+2C+2Cl2 ![]() TiCl4+2CO TiCl4 +2Mg
TiCl4+2CO TiCl4 +2Mg ![]() 2MgCl2+Ti �������� �Ȼ�ԭ��
2MgCl2+Ti �������� �Ȼ�ԭ��
��������
���ݹ�ҵ����ͼ�����ʷ����ԭ�����������������������������ʵ����ʼ�ת����ϵ��д��ط�Ӧ����ʽ���������ʹ�ҵ����ԭ��������ͼ�������
��1������1�Ƿ����Һ�������Է��������ǹ��ˣ����ò���������©�������������ձ����Լ������������ܽ�������þ�����Ȼ�þ��Һ������Ӧ�����ᣬ�ʴ�Ϊ��©�������������ձ� �� ���
��2�����Ȼ�þ��Һ�õ�����MgCl2��6H2OӦ���õķ���Ϊ�����ᾧ���ʴ�Ϊ�������ᾧ��
��3������ԭ���غ㣬�ҵõ�TiCl4��һ�ֿ�ȼ�����壬���Կ�ȼ������ΪCO����Ӧ�ķ���ʽΪ��TiO2+2C+2Cl2 ![]() TiCl4+2CO ���ʴ�Ϊ��TiO2+2C+2Cl2
TiCl4+2CO ���ʴ�Ϊ��TiO2+2C+2Cl2 ![]() TiCl4+2CO��
TiCl4+2CO��
��4����ϡ�������Χ�����£�þ��TiCl4��Ӧ�õ��Ѻ��Ȼ�þ����Ӧ�Ļ�ѧ����ʽΪ��TiCl4 +2Mg ![]() 2MgCl2+Ti�����ȵ������£�þ��ԭTiCl4�õ��ѣ����Ը÷�Ӧ�Ľ���ұ�����������Ȼ�ԭ�����ʴ�Ϊ��TiCl4 +2Mg
2MgCl2+Ti�����ȵ������£�þ��ԭTiCl4�õ��ѣ����Ը÷�Ӧ�Ľ���ұ�����������Ȼ�ԭ�����ʴ�Ϊ��TiCl4 +2Mg ![]() 2MgCl2+Ti�������������Ȼ�ԭ����
2MgCl2+Ti�������������Ȼ�ԭ����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о�Խ��Խ���ȡ������û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯���������.
(1)��ҵ���ں����ܱ������������з�Ӧ�ϳɼ״���CO(g)+2H2(g)![]() CH3OH(g) ��H
CH3OH(g) ��H
������������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶� | 250�� | 300�� | 350�� |
K | 2.041 | 0.270 | 0.012 |
���ɱ��������жϡ�H ________0 ( ���������� �� �� �� �� �� �� ��) ��
���жϷ�Ӧ�ﵽƽ��״̬��������________.
A.����CH3OH������������CO���������
B.��������ƽ����Է�����������
C.���������ܶȲ���
D.CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
�۽����ϱ������жϣ�Ҫ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��________.
A.���� B.�������H2 C.������״� D.�������
(2)CH3OH��������ȼ�ϵ�ص�ȼ�ϣ��Լ״��������ķ�ӦΪԭ����ƣ����е������Һ��KOH��Һ��ȼ�ϵ�ء���д���õ�ظ����ĵ缫��Ӧʽ��____________________.
(3)��BaSO4�����м��뱥��̼������Һ����ֽ��裬��ȥ�ϲ���Һ����˴�����Σ���ʹBaSO4ȫ��ת��ΪBaCO3��������Ӧ��BaSO4(s)+CO32-(aq)BaCO3(s)+SO42-(aq)����֪ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=4.0��10��2��BaSO4��Ksp=1.0��10��10���� BaCO3���ܶȻ�Ksp=________________��